" Bilim. Kanıt. Şifa. | Dr. Aleksi: Yeni Nesil Sağlık Ekosistemi."
Hastalıkların Evrimi ve Redoks Kodunun Sırrı: Neden Hala Hastayız?
Dr. Alexi
11/22/20257 min oku
Hastalıkların Evrimi ve Redoks Kodunun Sırrı: Neden Hala Hastayız?
Tıp Felsefesi ve Biyolojinin Kesişimi
Modern tıp, kardiyovasküler hastalık (KVH) gibi ölümcül patolojilere karşı etkili tedaviler geliştirerek (ABD'de 1960'lardan bu yana kalp hastalıklarından ölümlerin azalması gibi) büyük başarılar elde etti. Ancak günümüzde hala KVH, kanser ve metabolik bozukluklar, küresel ölüm nedenlerinin başında gelmektedir. Bu durum, bizi tıp felsefesinin temel sorusuna geri götürür: Hastalıklarımızın kök nedeni, sadece modern yaşam tarzı ve teknolojiden mi ibaret, yoksa biyolojik sistemlerimizde daha derin, evrimsel bir kusur mu var?
Antropolojik kayıtlar ve biyokimya, cevabın evrimsel adaptasyon ile çevresel maruziyetin kesiştiği noktada saklı olduğunu gösteriyor. Bu kesişim noktasının anahtarı ise Redoks Dengesidir.
I. Redoks Dengesizliği: Elektronların Yıkıcı Gücü
Redoks (Redüksiyon-Oksidasyon) Dengesizliği, vücudumuzdaki moleküller arasında kimyasal reaksiyonlar sırasında gerçekleşen elektron alışverişindeki bir bozukluğu tanımlar.
Oksidasyon: Bir molekülün elektron kaybetmesi (hasar görmesi).
Redüksiyon: Bir molekülün elektron kazanması (onarılması).
Redoks Dengesinin Önemi: Biyokimyasal homeostaz, bu iki aktivitenin uyum içinde sürmesine bağlıdır. Hücrelerimiz enerji üretirken kaçınılmaz olarak Reaktif Oksijen Türleri (ROS) üretir. Bu ROS (Süperoksit, Hidroksil radikali gibi serbest radikaller), eşleşmemiş elektronlara sahip olduğu için son derece reaktiftir. Normalde antioksidanlar, kendilerinden elektron vererek bu radikalleri nötralize eder.
Dengesizliğin Yıkımı: Eğer serbest radikaller, antioksidan kapasitesini aşarsa, oksidatif stres başlar. Bu durum, lipit peroksidasyonuna, proteinlerin konformasyonel modifikasyonuna ve en önemlisi DNA hasarına yol açar. Bu hücresel hasar, ateroskleroz, diyabet, nörodejenerasyon ve kanser gibi tüm kronik hastalıkların ortak paydasıdır.
II. Evrimsel Çelişki: Antik Çağ Hastalıkları ve Modern Yük
Eğer obezite, Tip 2 diyabet, ateroskleroz ve kanser gibi hastalıklar sadece elektromanyetik radyasyon (EMR), kirlilik veya modern beslenmeden kaynaklansaydı, teknoloji öncesi dönemde bu hastalıkların izine rastlanmamalıydı. Ancak antropolojik kayıtlar, bu varsayımı çürütmektedir:
Antik Kanser: Homininlerde kanserin en eski kanıtı, 1.98 milyon yıl öncesine dayanan Australopithecus sediba'nın omurunda bir osteojenik tümör olarak bulunmuştur. Eski Mısır mumyalarında (MÖ 3000-1500) rektum adenokarsinomu ve metastatik karsinom vakaları belgelenmiştir.
Antik Ateroskleroz: 5.300 yıl önce yaşamış Ötzi adı verilen Tirol buz adamında, karotid arterlerinde kireçlenme saptanmıştır. 4.000 yıllık insanlık tarihini inceleyen ünlü HORUS Çalışması, eski Mısırlı, Perulu ve Eskimolarda dahi ateroskleroz bulgularını ortaya koymuştur. Hatta Prenses Ahmose-Meryet-Amon, 3.500 yıl önce yaşamasına rağmen koroner arter hastalığı teşhisi konan ilk insandır.
Açıklama: Antik çağ insanları, düşük karbonhidrat içeren sağlıklı diyetlerle beslenmelerine ve EMR'ye maruz kalmamalarına rağmen neden hasta oldular? Cevap, Redoks Dengesindeki Evrimsel ve Çevresel Bozulmada gizlidir.
Evrimsel Adaptasyon: İnsan genomundaki bir genetik mekanizma, kıtlık dönemlerinde hayatta kalmak için beyaz yağ dokusunun (depo) artırılmasını ve insülin direnci geliştirilmesini sağlamıştır. Bu adaptasyon, bol gıdalı modern çağda obezite ve diyabeti hızlandırmaktadır.
Doğal Çevresel Stres: Antik çağda dahi, enfeksiyonlar, doğal toksinler, yüksek hayvansal yağ tüketimi veya besin döngüsündeki ani değişimler, o dönemki insanların Redoks dengesini bozmaya yetmiştir.
Peroksiredoksin Kodunu Çözmek: Hücresel Saat, Yaşlanma ve Kanser İkilemi
Hastalıkların Evrimi ve Redoks'un Temel Rolü
Hastalıkların evrimi ve yaygınlığı, sadece modern yaşam tarzıyla değil, Redoks Dengesizliği adı verilen temel bir biyokimyasal bozulmayla açıklanır. Redoks (Oksidasyon-Redüksiyon) dengesi, hücredeki elektron alışverişinin uyumunu temsil eder. Bu denge bozulduğunda (Oksidatif Stres), DNA ve proteinlere hasar veren Reaktif Oksijen Türleri (ROS) artar. Bu hücresel yıkım, ateroskleroz, diyabet ve kanser gibi kronik hastalıkların patogenezinde ortak bir zemin oluşturur. Bu biyolojik karmaşanın merkezinde ise, Redoks durumunu düzenleyen Peroksiredoksin (PRDX) enzim ailesi yer alır.
I. PRDX: Hücresel Saatin Antik Mekanizması
PRDX, arkilerden insanlara kadar tüm canlı organizmalarda bulunan, yaklaşık 2.45 milyar yıl öncesine uzanan çok antik ve çok işlevli bir enzim ailesidir.
A. Redoks Sirkadiyen Sistemi
PRDX'in en çarpıcı rolü, sadece bir antioksidan değil, aynı zamanda hücrenin zamanlamasını yöneten bir "alternatif sirkadiyen sistem" oluşturmasıdır.
Mekanizma: PRDX'in ritmik çalışması, doğrudan Redoks durumu ile yönetilir. Enzim, zararlı hidrojen peroksiti (H2O2) zararsız suya indirgerken (redüksiyon) kendisi oksitlenir. Bu sürekli oksidasyon-redüksiyon döngüsü, biyolojik zamanlamanın temelini oluşturur.
Bağlantı: Bu döngü, fotoreseptörleri olmayan basit organizmaların bile çevresel değişimleri (mavi ışık, ROS) algılayarak biyolojik zamanlamalarını korumasını sağlar. PRDX'ten gelen bu zaman sinyalleri bozulduğunda, transkripsiyonel sirkadiyen saat genlerinin (PER, CRY) ritmi de etkilenir. Bu sirkadiyen kargaşa, kanser, Tip 2 diyabet ve nörodejenerasyon gibi durumları moleküler düzeyde hızlandırır.
Evrimsel Çıkarım: Antik çağlarda dahi doğal çevresel stresörler ve evrimsel beslenme çelişkileri nedeniyle oluşan sürekli oksidatif stres, bu Redoks ritmini bozmaya yetmiştir. Günümüzde ise EMR ve yapay ışık kirliliği, PRDX sistemini aşırı yükleyerek bu yıkımı hızlandırmaktadır.
B. PRDX'in Çok Yönlü Fonksiyonları (Moonlighting)
PRDX, aktif merkezindeki sistein kalıntısının farklı redoks durumlarına geçebilme yeteneği sayesinde antioksidanlığın ötesinde roller üstlenir:
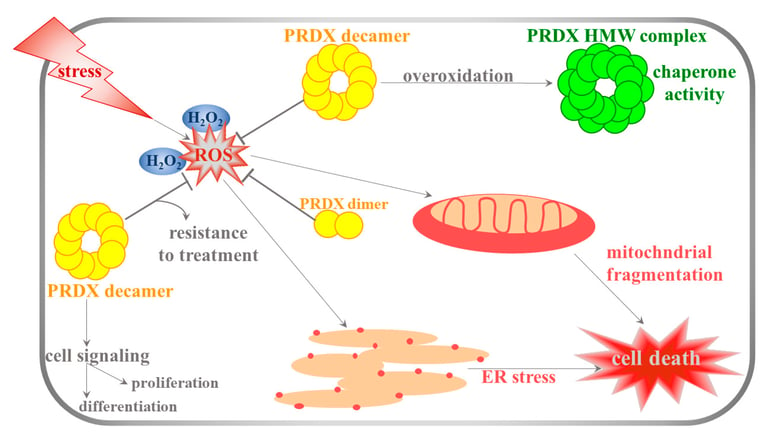
Şaperon Aktivitesi: Oksitlendiklerinde, PRDX molekülleri birleşerek büyük kompleksler oluşturur ve yanlış katlanmış proteinlerin toplanmasını ve onarılmasını sağlayan şaperonlara dönüşür. Bu, hücresel stresi ve yaşlanmayı önler.
Redoks Sinyal Regülatörü: Serbest radikal seviyelerini düzenleyerek, PTEN gibi tümör baskılayıcı proteinlerin oksidasyonunu engeller ve hücre büyümesini durduran sinyal yollarının aktif kalmasını sağlar.
Hücre Döngüsü Kontrolü: PRX'ler, hücre döngüsü proteinlerini fosforlayarak veya oksitleyerek hücrenin bir sonraki faza geçişini düzenlerler.
II. PRDX ve Kronik Patoloji İkilemi
A. Yaşlanma (Senescence) ve Hücresel Savunma
PRDX aktivitesindeki azalma, tüm organizmalarda yaşlanma sürecini hızlandırır.
Telomer ve DNA Korunması: PRX1, kromozom uçlarında yoğunlaşarak ROS kaynaklı telomer hasarını önler ve telomer kısalmasını yavaşlatır. Ayrıca oksidize DNA hasarının birikmesini engelleyerek telomeraz aktivitesini destekler.
Mitokondriyal Savunma: PRX3, Mitokondriyal Redoks dengesini korumada esastır. PRX3'teki azalma Mitokondriyal Disfonksiyonu artırarak kas atrofisi (sarkopeni) ve kronik yorgunluk gibi yaşlanma süreçlerini hızlandırır.
Senescence Baskısı: PRX'ler, hücreleri yaşlanmaya iten tümör baskılayıcı protein p16 ekspresyonunu azaltarak hücresel yaşlanmayı önlemeye yardımcı olur.
B. Kanser Çelişkisi: Onkoprotein mi, Baskılayıcı mı?
PRDX'in kanserdeki rolü çelişkilidir:
Tümör Baskılayıcı Rolü: PRX1, c-Abl ve c-Myc gibi kanser gelişimini destekleyen onkoproteinleri inhibe ederek hücre büyümesini durdurur ve oksidatif DNA hasarına karşı hassasiyeti azaltır.
Onkoprotein Rolü: Çoğu kanser hücresi, PRDX'i yüksek düzeyde üretir. Bu, PRDX'in kanser hücreleri için bir hayatta kalma güçlendiricisi olarak hareket ettiğini gösterir. PRDX, kanser hücrelerini kemoterapi ve aşırı oksidatif stresten koruyarak metastazı ve kemorezistansı (ilaç direncini) teşvik eder.
III. Terapötik Çözümler ve Gelecek Perspektifi
Redoks dengesindeki bozulma geri döndürülebilir olduğundan, tedavi yaklaşımları hücresel savunmayı güçlendirmeye odaklanır:
Nrf2 Aktivasyonu: Nrf2, hücrenin antioksidan savunma yollarının ana anahtarıdır. Sülforafan ve Kurkumin gibi doğal bileşikler Nrf2'yi aktive ederek Glutatyon üretimini ve detoks enzimlerini artırır. Bu, PRDX enzimlerinin verimli çalışması için gerekli ortamı sağlar.
Modülatör Destekleri: Vücudun endojen (içsel) antioksidanlarını desteklemek kritik öneme sahiptir:
Glutatyon/NAC: PRDX'in yenilenmesini sağlayan temel destektir.
C Vitamini: Glutatyon sentezine yardımcı olur.
Ürik Asit: Yüksek konsantrasyonlarda antioksidan olabilir, ancak aşırı yükselmesi (Hiperürisemi) pro-inflamatuar etki göstererek damar hasarını artırabilir.
PRDX İnhibitörleri: Kanser hücrelerinin hayatta kalmasını sağlayan PRDX'i hedef alan adenanthin gibi inhibitörler, yeni kanser tedavileri için umut vericidir, ancak güvenlik ve spesifiklikleri klinik araştırmalarla netleştirilmelidir.
Sağlıklı yaşlanmak ve kronik hastalıklara karşı direnmek, sadece çevresel toksinleri suçlamakla değil, Peroksiredoksin salınımlarını ve Redoks sirkadiyen sistemimizdeki ince dengeyi moleküler düzeyde korumakla mümkündür.
Mitokondriyal Redoks Yönetimi ve Terapötik Bileşikler
Hedef: Mitokondrinin ROS üretimini azaltmak ve enerji verimliliğini artırmak.
Destekler: Alfa Lipoik Asit (ALA), hem suda hem yağda çözünebilen bir antioksidan olarak Mitokondri zarını korur ve Glutatyon'u geri dönüştürür. Koenzim Q10 (CoQ10) ise Mitokondriyal elektron taşıma zincirinde hayati rol oynayarak ATP üretimini destekler. Bu bileşenler, Redoks döngüsünü Mitokondri düzeyinde yöneterek enerji yetersizliğini ve sarkopeni gibi yaşlanma süreçlerini yavaşlatır.
Polifenoller ve Eser Elementler: Kofaktör ve Çözücü Rolü
Polifenoller: Quercetin ve Resveratrol gibi polifenoller, sadece serbest radikal süpürücüsü olarak değil, aynı zamanda Metilasyon ve Redoks döngülerinde yer alan enzimleri destekleyerek etki ederler.
Eser Elementler: Çinko ve Selenyum, Glutatyon peroksidaz gibi ana antioksidan enzimlerin kofaktörleridir. Bu eser elementlerin eksikliği, doğrudan antioksidan savunma kapasitesini düşürür ve Redoks dengesizliğini körükler.
Biyo-yararlanım: Bu terapötik ajanların etkinliği, hücresel hedeflere ne kadar ulaştığına bağlıdır. Lipozomal formülasyonlar veya fitozom teknolojisi gibi yüksek biyoyararlanıma sahip formların kullanımı, bu moleküler hedeflere ulaşmada kritik öneme sahiptir.
Doris Loh
Bağımsız araştırmacı – Kuantum biyolojisi; Redox, EMF ve VitC
