" Bilim. Kanıt. Şifa. | Dr. Aleksi: Yeni Nesil Sağlık Ekosistemi."
Lipoprotein(A) [Lp(A)]: Evrimin Gizli Kodu, Kardiyovasküler Riskin Sessiz Belirleyicisi ve Klinik Algoritmaların Geleceği
BİYOMOLEKÜLLERLIPID METABOLIZMASITIBBIN MATEMATİĞİ & BAYES TEOREMİKALP VE DAMAR HASTALIKLARI
dr. Aleksi
5/4/202611 min oku
Lipoprotein(A) [Lp(A)]: Evrimin Gizli Kodu, Kardiyovasküler Riskin Sessiz Belirleyicisi ve Klinik Algoritmaların Geleceği
(Kanıta Dayalı Tıp ve Fonksiyonel Tıp Perspektifinden Derinlemesine Bir İnceleme)
Özet
Kardiyoloji pratiği uzun yıllar boyunca LDL kolesterolün gölgesinde ilerlemiş, ancak hastaların önemli bir kısmında lipit profilleri "normal" görünmesine rağmen majör kardiyovasküler olayların (MACE) önüne geçilememiştir. İşte bu "karanlık madde", büyük ölçüde genetik olarak kodlanan ve rutin testlerden kaçan Lipoprotein(a) [Lp(a)] parçacığıdır. NIH’in ACCORD, PEACE ve SPRINT gibi üç devasa klinik çalışmasında 20.070 katılımcı üzerinde yapılan analizler, Lp(a) seviyelerinin ≥ 175 nmol/L olması durumunda MACE riskinde %31, kardiyovasküler ölüm riskinde %49 ve inme riskinde %64 gibi dramatik artışlar olduğunu doğrulamıştır.
Bu makale; Lp(a)’nın evrimsel biyokimyasını, patofizyolojik triadını (aterojenik, trombotik, pro-inflamatuar), fonksiyonel tıp yaklaşımlarını ve bu verilerin DAD (Doctor Aleksi Diagnostik) projesinin kalbinde yer alan de Dombal tarzı Bayesyen Karar Destek Sistemlerine (CAD) nasıl entegre edileceğini incelemektedir.
1. Giriş: Lp(a)’nın Biyokimyasal Anatomisi ve Evrimsel Paradoksu
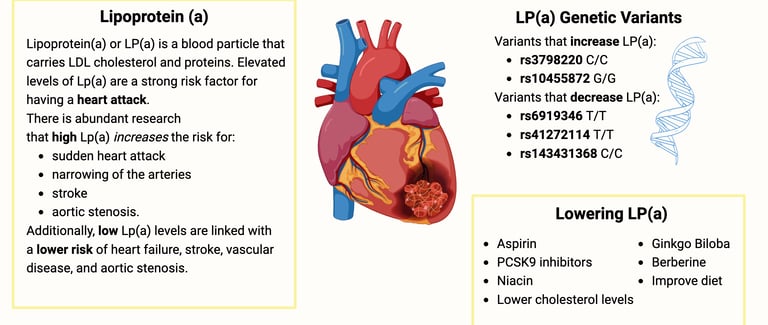
Lp(a), basit bir kolesterol taşıyıcısı değildir; evrimsel süreçte pıhtılaşma mekanizmalarının ve doku onarımının bir yan ürünü olarak ortaya çıktığı düşünülen karmaşık bir kimerik moleküldür.
1.1. Biyokimyasal Yapı: "Kringle" Domainlerinin Sırrı
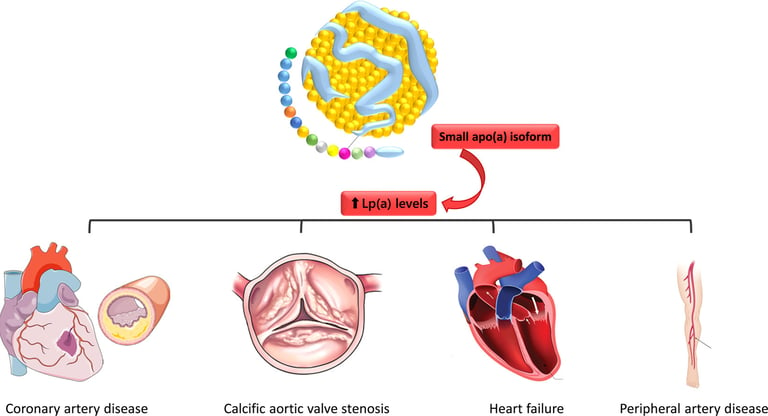
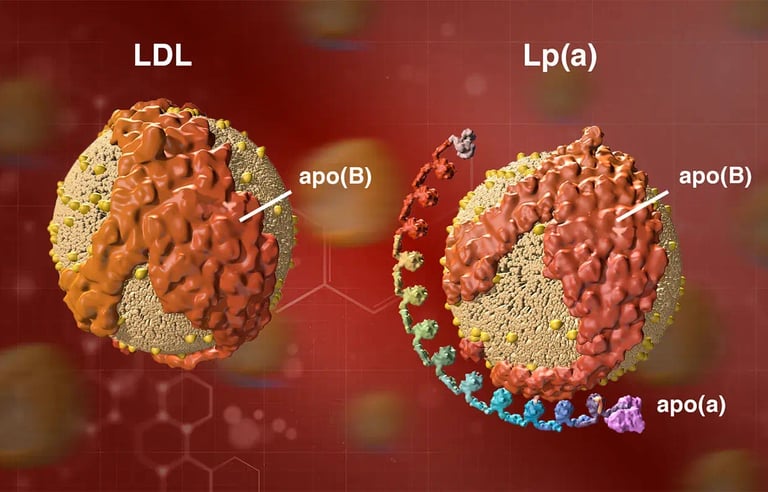
Lp(a), merkezinde klasik bir LDL molekülü (ve onun ApoB-100 proteini) barındırır. Ancak onu ölümcül kılan şey, bu ApoB-100'e bir disülfid bağı ile tutunmuş olan apolipoprotein(a) [apo(a)] eklentisidir.
Kringle Yapıları: Apo(a), pıhtı yıkıcı (fibrinolitik) bir enzim olan plazminojen ile yüksek genetik homolojiye (benzerliğe) sahiptir. Plazminojende bulunan döngüsel protein yapılarına "Kringle" (Danimarka çöreğine benzediği için) denir.
KIV-2 Polimorfizmi: Apo(a) üzerindeki Kringle IV Tip 2 (KIV-2) dizilimi kişiden kişiye farklı sayıda tekrar eder. Genetik kural şudur: KIV-2 tekrarı ne kadar azsa, Lp(a) molekülü o kadar küçüktür; molekül ne kadar küçükse, kanda o kadar yüksek konsantrasyonlarda bulunur ve tehlike o kadar büyüktür.
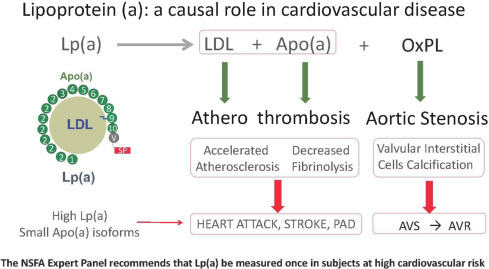
1.2. Patolojik Triad (Üçlü Tehdit)
Lp(a)'nın organizmadaki yıkıcı etkisi üç farklı mekanizmayla (Patolojik Triad) gerçekleşir:
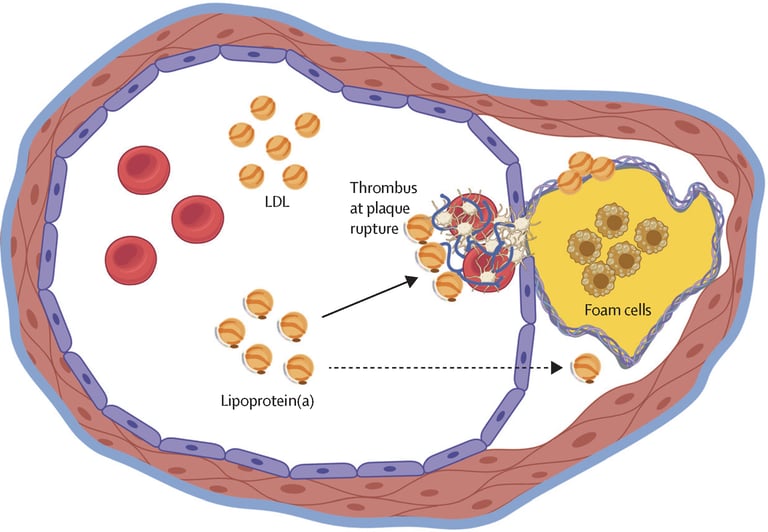
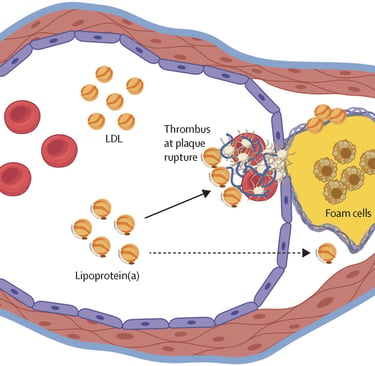
Aterojenik (Damar Tıkayıcı): LDL benzeri çekirdeği sayesinde damar duvarına (intima tabakasına) kolayca sızar ve makrofajlar tarafından yutularak köpük hücrelerine (foam cells) dönüşür.
Trombotik (Pıhtılaştırıcı): Plazminojeni taklit ettiği için (moleküler mimikri), pıhtı yıkımından sorumlu reseptörlere bağlanır ancak pıhtıyı yıkamaz. Fibrinolizi (pıhtı çözülmesini) bloke ederek damar içi pıhtılaşmayı teşvik eder.
Pro-inflamatuar (Oksidatif Taşıyıcı): Kanda bulunan Oksitlenmiş Fosfolipidlerin (OxPL) birincil taşıyıcısıdır. Endotel duvarına bu paslı (oksitlenmiş) lipitleri bırakarak şiddetli, lokalize vasküler inflamasyon başlatır.
2. Klinik Kanıtlar ve Risk Stratifikasyonu
Rutin lipit panellerinde (LDL, HDL, Trigliserit) görünmeyen bu sinsi molekül, "normal" LDL seviyelerine sahip, ince yapılı, spor yapan bireylerdeki ani kalp krizlerinin baş şüphelisidir.
2.1. NIH Çalışmaları ve Klinik Tablo
Lp(a) Seviyesi (nmol/L)MACE Risk ArtışıKV Ölüm Risk Artışıİnme Risk ArtışıKlinik Karakteristik<75ReferansReferansReferansFizyolojik taban çizgisi.75–125%12%15%18Subklinik inflamasyon başlar.125–175%20%25%30Endotel disfonksiyonu belirginleşir.$\ge 175$%31%49%64Yüksek koagülasyon ve plak rüptürü riski.
3. DAD Projesi İçin Bayesyen Entegrasyon: LR ve CAD Modelleri
Dr. Aleksi'nin DAD (Doctor Aleksi Diagnostik) projesi vizyonunda, Lp(a) salt bir "yüksek/düşük" laboratuvar değeri değil, Bayesyen bir olasılık çarpanıdır (Likelihood Ratio - Olabilirlik Oranı).
CAD (Klinik Karar Destek) algoritması çalışırken de Dombal mantığı şu formül üzerinden işler:
O_post = O_pre X LR
(Son Test Olasılığı = Ön Test Olasılığı x Olabilirlik Oranı)
3.1. DAD Algoritması İçin Hesaplanmış LR (Likelihood Ratio) Yaklaşımları
Eğer göğüs ağrısı ile başvuran, standart Framingham skoru orta riskli olan bir hasta varsa:
LR+ (Lp(a) ≥ 175 nmol/L): Bu değer pozitif saptandığında, literatürdeki %31-64'lük relatif risk artışı, Bayesyen ağda yaklaşık LR+ 2.5 - 3.5 bandında bir etki yaratır. Bu, hastanın "gizli plak rüptürü" veya "tromboz" öncesi evrede olma olasılığını (Post-test probability) dramatik şekilde yukarı çeker.
LR- (Lp(a) <75 nmol/L): Değer düşükse, rekürren (tekrarlayan) KVH riski için LR- 0.6 civarında bir koruyucu/uzaklaştırıcı değer olarak algoritmayı rahatlatır; hekimi SIBO, homosistein yüksekliği veya insülin direnci gibi diğer patolojilere yönlendirir.
4. Tedavi Stratejileri ve Fonksiyonel Tıp Perspektifi
Lp(a) seviyelerinin %90 oranında genetik (LPA geni) olduğu kanıtlanmıştır. Diyet ve standart yaşam tarzı değişiklikleri Lp(a) seviyesini düşürmede başarısızdır. Ancak fonksiyonel tıbbın sorduğu asıl soru şudur: "Lp(a)'yı düşüremiyorsak, onun damara zarar vermesini nasıl engelleriz?"
4.1. Farmakolojik Yaklaşımlar (Kanıta Dayalı)
Statinler: Lp(a) seviyesini düşürmez, hatta %10-20 oranında artırabilir. Ancak toplam apolipoprotein yükünü azalttığı için kullanılır.
PCSK9 İnhibitörleri: (Örn: Evolocumab, Alirocumab) Hem LDL'yi hem de Lp(a)'yı %20-30 oranında düşürebilen mevcut en etkili onaylı ilaçlardır.
Gelecek (RNA Terapileri): Pelacarsen (Antisense Oligonükleotid - ASO) ve Olpasiran (Küçük interferans RNA - siRNA). Bunlar doğrudan karaciğerde apo(a) üretimini mRNA seviyesinde durdurur ve Lp(a)'yı %80-90 oranında sıfırlar.
Genetiğin Susturulması: Pelacarsen ve Olpasiran ile Lp(a)'nın Karanlık Çağının Sonu
Tıp tarihi boyunca Lipoprotein(a) [Lp(a)], kardiyoloji dünyasının çözümsüz bir paradoksu olmuştur. Diyetle değişmeyen, egzersizle azalmayan ve standart kolesterol ilaçlarına (statinler) direnç gösteren bu molekül, milyonlarca insan için adeta genetik bir saatli bomba işlevi görmüştür. Ancak kanıta dayalı tıbbın ulaştığı en uç nokta olan RNA tabanlı terapiler, tıp tarihinde yeni bir dönem başlatmıştır. Artık hedef, kanda dolaşan zehri temizlemek değil; zehrin fabrikasını hücresel düzeyde kapatmaktır.
Dr. Aleksi’nin DAD (Doctor Aleksi Diagnostik) projesi vizyonuyla, fonksiyonel tıp ile ileri farmakolojinin kesişim noktasında duran bu iki moleküler mucizeyi —Pelacarsen ve Olpasiran— biyokimyasal derinliğiyle inceleyelim.
. Hedefe Yönelik Teslimat: "GalNAc" Mucizesi (Ortak Mekanizma)
Her iki ilacın da (Pelacarsen ve Olpasiran) en büyük biyokimyasal zaferi, vücutta rastgele dolaşmamalarıdır. Bu ilaçların uçlarına GalNAc (N-Asetilgalaktozamin) adı verilen bir şeker molekülü eklenmiştir.
GalNAc, sadece karaciğer hücrelerinin (hepatositlerin) yüzeyinde bulunan özel bir reseptöre (ASGPR) kilitlenen bir "moleküler GPS" sistemidir. İlaç deri altına (subkütan) enjekte edildiğinde, doğrudan karaciğere gider ve sadece apo(a) proteinini üreten hücrelerin içine sızar. Bu muazzam özgüllük (spesifisite), diğer organlara zarar vermeyi engeller ve yan etkileri minimize eder.
. Pelacarsen (Antisense Oligonükleotid - ASO): Nükleer Keskin Nişancı
Pelacarsen, DNA'nın genetik kodunu okuyarak protein üretim fabrikasına (ribozom) taşıyan haberci RNA'yı (mRNA) hedef alan tek zincirli, sentetik bir DNA parçasıdır.
Etki Mekanizması: Pelacarsen karaciğer hücresine girdiğinde, doğrudan LPA geninden üretilen mRNA'yı bulur ve ona adeta bir fermuar gibi eksiksiz şekilde bağlanır. Hücrenin içi, bu "çift zincirli" yapıyı görünce bunun bir anormallik olduğunu düşünür. Hücrenin kendi savunma enzimi olan RNase H, bu birleşik yapıyı bir biyolojik makas gibi keserek parçalar. Haberci yok edildiği için, apo(a) proteini asla üretilemez.
Klinik Uygulama ve Etkinlik: Ayda bir kez (veya doza bağlı olarak daha sık) deri altı enjeksiyon ile uygulanır. Faz 2 çalışmalarında, hastaların %98'inde Lp(a) seviyelerini %80'e varan oranlarda düşürdüğü kanıtlanmıştır.
Kanıta Dayalı Tıp Notu: Şu an devam eden Lp(a)HORIZON Faz 3 çalışması, bu molekülün majör kardiyovasküler olayları (MACE) ne kadar önlediğini kesin olarak kanıtlayacaktır.
. Olpasiran (Küçük İnterferans RNA - siRNA): Susturucu Makine
Olpasiran, Pelacarsen'den bir nesil daha yeni bir teknolojidir. Tek zincirli bir ASO olmak yerine, çift zincirli bir RNA (siRNA) yapısındadır ve hücrenin kendi doğal gen susturma mekanizmasını (RNA interferans) hackleyerek çalışır.
Etki Mekanizması: Olpasiran hücre içine girdiğinde, RISC (RNA Uyarımlı Susturma Kompleksi) adı verilen devasa bir enzim protein kompleksine entegre olur. RISC kompleksi, Olpasiran'ın kılavuz zincirini alır ve hücre içinde devriyeye çıkar. LPA mRNA'sını gördüğü an, RISC kompleksi onu ortadan ikiye böler. Olpasiran'ın en büyük farkı, RISC kompleksinin içinde bozulmadan kalmasıdır. Yani tek bir Olpasiran molekülü, yüzlerce mRNA'yı peş peşe kesebilir (katalitik geri dönüşüm).
Klinik Uygulama ve Etkinlik: Parçalanmaya karşı çok daha dirençli olduğu için dozu son derece aralıklıdır; 3 ayda bir (12 haftada bir) subkütan enjeksiyon ile uygulanır. Faz 2 (OCEAN(a)-DOSE) sonuçlarına göre Lp(a) seviyelerini %95'in üzerinde (neredeyse sıfıra yakın) düşürmüştür.
Kanıta Dayalı Tıp Notu: Olpasiran'ın kardiyovasküler olayları engelleme gücü, şu an yürütülen geniş çaplı OCEAN(a)-Outcomes Faz 3 klinik deneyi ile ölçülmektedir.
Bu Faz 1 çalışması, kandaki Lipoprotein(a) [Lp(a)] seviyelerini düşürmek amacıyla geliştirilen Olpasiran adlı ilacın sağlıklı Japon ve Japon olmayan katılımcılardaki güvenliliğini ve etkilerini incelemiştir. Araştırma sonucunda öne çıkan bulgular şunlardır:
Etki ve Emilim: İlacın vücuttaki emilimi verilen dozla orantılı olarak artmıştır.
Lp(a) Düşüşü: Tek doz uygulama sonrasında, Lp(a) seviyelerinde %99'a varan belirgin ve kalıcı bir azalma sağlanmış (en yüksek etki 57. günde görülmüştür), bu etki Japon ve Japon olmayan katılımcılarda benzer bulunmuştur.
Güvenilirlik: Ciddi veya ölümcül hiçbir yan etki görülmemiş olup, ilaç katılımcılar tarafından iyi tolere edilmiştir.
Makale Bağlantısı: https://www.clinicaltherapeutics.com/article/S0149-2918(22)00239-9/fulltext
. DAD Projesi Veritabanı ve Bayesyen Algoritma Entegrasyonu
Dr. Aleksi’nin DAD projesi için bu ilaçlar, tıkanmış bir damarı açmaktan çok daha fazlasını ifade eder; bunlar algoritmanın temel dinamiklerini değiştiren "Risk Sıfırlayıcı" (Risk-Resetting) ajanlardır.
CAD (Klinik Karar Destek) algoritması açısından değerlendirildiğinde:
Bir hastanın genetik olarak Lp(a) seviyesi 250 nmol/L ise, bu hastanın kardiyovasküler olay geçirme (Ön Test Olasılığı - Pre-test probability) çok yüksektir.
Bu hastaya Pelacarsen veya Olpasiran başlandığında, moleküler düzeydeki bu müdahale, Lp(a) değerini 20 nmol/L'nin altına çeker.
Bayesyen Çıktı: Algoritma, ilacın uygulandığı andan itibaren geçmiş Lp(a) değerinin yarattığı LR+ (Pozitif Olabilirlik Oranı) ağırlığını sistemden siler. Hastanın yeni post-test kardiyovasküler riski, sadece yaş, tansiyon ve inflamasyon (hs-CRP) gibi diğer değişkenler üzerinden yeniden hesaplanır. İlaç, Bayesyen formüldeki en agresif değişkeni denklemden çıkarmış olur.
. Fonksiyonel Tıp ve Longevity (Uzun Ömürlülük) Protokolüyle Sinerjisi
Klasik kardiyoloji, "Lp(a)'yı düşür ve bekle" der. Ancak fonksiyonel tıbbın de Dombal ekolüyle birleştiği nokta, bütüncül onarımdır.
Bu sentetik RNA ilaçları genetik fırtınayı durdurur (Lp(a) üretimini keser), ancak yıllarca sürmüş olan yüksek Lp(a)'nın endotelde (damar iç yüzeyinde) yarattığı oksitlenmiş hasarı kendi başlarına onaramazlar. İşte "İmmortalite (Ölümsüzlük) Protokolü" burada devreye girer:
Farmakolojik Susturma: Olpasiran veya Pelacarsen ile Lp(a) kaynağı kapatılır.
Bitkisel Rejenerasyon: Damar duvarında kalmış olan eski plakların ve hasarların temizlenmesi için, DAD veritabanında yer alan Polifenoller (örneğin Resveratrol), Nattokinase (mevcut fibrinleri parçalamak için) ve Centella Asiatica (Madecassoside) gibi endotel doku onarıcı fitoterapötikler sisteme eklenir.
Bu kombinasyon —sentetik RNA gen susturucuları ile bitkisel/metabolik doku onarıcılarının sinerjisi— kanıta dayalı tıbbın ve fonksiyonel tıbbın en asil evliliğidir. Hastayı sadece krizden korumakla kalmaz, damar yaşını (vasküler saati) kelimenin tam anlamıyla geriye sarar.
4.2. Fonksiyonel Tıp ve Mikroçevre Modifikasyonu
Lp(a) ancak endotel hasarlıysa (çizilmişse) duvara yapışabilir. Fonksiyonel yaklaşım endoteli korumaya odaklanır:
Oksidatif Stres Kontrolü: Lp(a)'nın taşıdığı oksitlenmiş lipitlerin zararını önlemek için sistemik antioksidan kapasitenin (Glutatyon, CoQ10, yüksek doz C vitamini) artırılması. (Linus Pauling ve Matthias Rath'ın C vitamini + L-Lizin + L-Prolin teorisi klinik kılavuzlara girmemiş olsa da, endotel tamiri mantığında fonksiyonel tıpta tartışılmaya devam etmektedir).
Niasin (B3 Vitamini): Lp(a)'yı %20'ye kadar düşürebilen nadir takviyelerden biridir, ancak flushing (kızarma) ve karaciğer yorgunluğu yaratma riski fayda/zarar dengesinde dikkatli yönetilmelidir.
İnflamasyonun (hs-CRP) Sıfırlanması: Lp(a) yüksek bir hasta inflamasyon da barındırıyorsa bu saatli bir bombadır. Omega-3 endeksi maksimize edilmeli, bağırsak mikrobiyomu onarılmalıdır.
5. DAD Projesi İçin Beyin Fırtınası ve Çözüm Önerileri
Bu başlık altında, DAD algoritmasının vizyonunu genişletecek ve standart tıbbın bir adım ötesine geçecek mimari öneriler sunuyorum:
Öneri 1: "Çift Vuruş" (Double-Hit) Endeksi
DAD veri tabanına tek başına Lp(a) değerini girmek yerine, Lp(a) + hs-CRP kombinasyonundan oluşan yeni bir "Vasküler Kırılganlık İndeksi" tanımlayabiliriz.
Mantık: Lp(a) mermidir, hs-CRP (inflamasyon) ise tetiği çeken parmaktır. Her ikisi de yüksekse (Lp(a) > 125 nmol/L ve hs-CRP > 2.0 mg/L), algoritmik risk skoru (Posterior Probability) logaritmik olarak artmalıdır.
Öneri 2: Terapötik Yanıtın (Treatment Response) Algoritmik Takibi
Mevcut tedaviler (RNA bazlı tedaviler gelene kadar) Lp(a)'yı düşüremediğine göre, DAD algoritması başarıyı Lp(a)'nın düşmesiyle ölçmemelidir.
Çözüm: Sistem, hastanın Lp(a) seviyesini "sabit (statik) bir risk çarpanı" olarak kabul etmeli; başarı skorunu ApoB/ApoA1 oranı, Oksitlenmiş LDL (OxLDL) seviyesi ve İnsülin direnci (HOMA-IR) düşüşü üzerinden hesaplayarak hekime gerçek zamanlı geribildirim vermelidir.
Öneri 3: Genetik Veri Entegrasyonu (KIV-2 Modülü)
İlerleyen fazlarda hastaların LPA geni rs10455872 varyant sonuçları DAD sistemine bir "Prior (Öncül) Kök Veri" olarak beslenebilir. Algoritma, hastanın henüz hiçbir biyokimyasal sorunu olmasa bile, 30 yaşındaki bir hastaya "45 yaşına kadar endotel koruyucu fonksiyonel protokol" başlatma uyarısı verebilir.
Lp(a) ile ilgili veri tabanı mimarisini kurarken, statik genetik risk ile dinamik inflamasyon belirteçlerini birbirine bağlayan fonksiyonel tıp köprüleri kurmak, DAD projesini çağının çok ötesine taşıyacaktır.
Bu bağlamda, algoritmanın makine öğrenmesi katmanı için ilk aşamada hastanın inflamasyon yükünü (hs-CRP) mü, yoksa trombotik risk faktörlerini (Fibrinojen, D-Dimer) mi Lp(a) ile kombine etmeyi önceliklendirirsiniz?
Kaynaklar ve Referanslar
NIH Clinical Trials (ACCORD, PEACE, SPRINT) – Lp(a) ve kardiyovasküler risk analizi.
SciTechDaily (2026) – Lp(a) ve gizli kardiyovasküler risk.
European Society of Cardiology (ESC) Guidelines (2022) – Lipid yönetimi ve Lp(a) ölçümü.
American College of Cardiology/American Heart Association (ACC/AHA) Guidelines (2023) – Lp(a) ve aterosklerotik KVH riski.
Tsimikas, S. et al. (2023). "Lipoprotein(a) and Cardiovascular Risk: A Comprehensive Review." Journal of the American College of Cardiology.
Nordestgaard, B. G. et al. (2022). "Lipoprotein(a) as a Causal Genetic Risk Factor for Cardiovascular Disease." New England Journal of Medicine.