" Bilim. Kanıt. Şifa. | Dr. Aleksi: Yeni Nesil Sağlık Ekosistemi."
Parkinson hastalığı & Dopamin Yönetimi
Parkinson hastalığı, dopamin seviyelerinin düşmesine neden olan beyin sinir hücre hasarının yol açtığı, elde titreme ile başlayan, kas sertliği yanı sıra denge kaybı gibi kontrolün bulunmadığı belirtiler gösteren ve yavaş ilerleyen nörolojik bir hastalıktır.
HASTALIK & SENDROMKRONİK HASTALIKLARBEYİN VE SİNİR HASTALIKLARIGERİARTRİ (YAŞLILIK TIBBI)NÖRO BİLİŞSEL RESTORASYON & NÖROPROTEKTİF
Dr. Aleksi
12/2/202510 min oku
PARKİNSON HASTALIĞI, DOPAMİN YÖNETİMİ VE REJENERASYON VİZYONU
1. TANIM VE FİZYOPATOLOJİ:
Parkinson Hastalığı (PH), beynin hareketleri kontrol eden devrelerinde "yakıt" görevi gören dopaminin azalmasıyla ortaya çıkan, ilerleyici bir nörodejeneratif bozukluktur.
Parkinson hastalığı (PH) ve hareket arasındaki karmaşık ilişkiyi tanımlayan, hastalığın özünü ve belirtilerini vurgulayan birkaç açıklama:
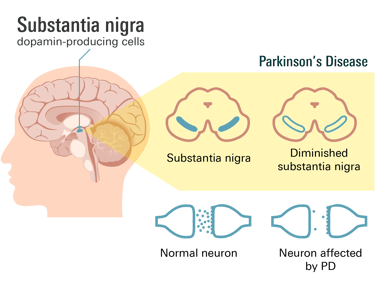
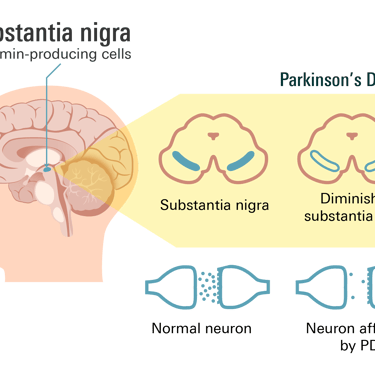
Parkinson, beynin Substantia Nigra bölgesindeki dopamin üreten nöronların kaybı nedeniyle hareketleri yumuşatan ve koordine eden sinyallerin (dopamin) azalmasıyla karakterize edilen, ilerleyici bir nörolojik hastalıktır.
Hastalığın hareket üzerindeki temel yansıması, beynin "gaz ve fren" sistemi arasındaki dengenin bozulmasıdır; bu durum, hareketin başlatılmasında (Bradikinezi) ve akıcılığında (rijidite) ciddi yavaşlamaya neden olur.
PH'nin en bilinen ayırt edici motor belirtileri; dinlenme halinde ortaya çıkan titreme (Tremor), hareketlerdeki genel yavaşlık (Bradikinezi) ve kaslardaki sertlik (Rijidite) olmak üzere üç ana başlıkta toplanır.
Dopamin eksikliği, beynin hareket devrelerinde kilit rol oynayanStriatum'a yeterli "yakıt" (dopamin) ulaşmasını engeller, bu da günlük aktivitelerde zorlanmaya, denge kaybına (Postüral İnstabilite) ve yürüyüş bozukluklarına yol açar.
A. Hastalığın Özü: Substantia Nigra'nın (Yavaş) Yıkımı
PH'nin temel patolojik olayı, beynin derinliklerinde yer alan Substantia Nigra (Siyah Madde) bölgesindeki dopamin üreten nöronların giderek kaybı ile seyretmesidir. Dopamin, hareketin akıcı ve koordineli olmasını sağlayan kilit nörotransmitterdir. Bu hücrelerin ölümü, beynin Striatum bölgesinde dopamin seviyesini düşürerek hareket devreleri arasındaki fren–gaz dengesini bozar ve hareketin yavaşlamasına yol açar.
B. Patolojinin Moleküler İmzası
Nöron kaybı, Alfa-Sinüklein adı verilen bir proteinin yanlış katlanması ve hücre içinde çözünmez topaklar halinde birikmesiyle (Lewy Cisimcikleri) ilişkilidir. Bu birikim, nöronun normal işleyişini bozarak ölümüne sürükler. Hastalığın seyrini etkileyen diğer faktörler arasında beyin–bağırsak eksenindeki (mikrobiyot) değişiklikler ve nöroinflamasyon yer alır.
2. KLİNİK BELİRTİLER, TANI ve PROGNOZ
Dopamin eksikliği, hastalığın hem motor (hareket) hem de non-motor (hareket dışı) semptomlarını ortaya çıkarır.
Motor Semptomlar (Temel Üçleme) Tremor (ellerde para sayar gibi bir istirahat titremesi, genellikle tek taraflı başlar), Bradikinezi (hareketlerde yavaşlama, ayaklarını kaldırmadan küçük adımlarla yürüme), Rijidite (kas sertliği), Postüral İnsatibilite (denge bozukluğu).
Non-Motor Semptomlar: Koku duyusunda azalma (genellikle erken belirtidir), kabızlık, REM uyku davranış bozukluğu, depresyon/anksiyete ve bilişsel etkilenme (ileri aşamalarda).
Prognoz (Hastalığın Gidişi): PH ilerleyicidir. Başlangıçta ilaçlara iyi yanıt görülse de, uzun vadede dalgalanmalar (wear-off), diskinezi (istem dışı hareketler) ve motor dışı belirtiler artabilir.
Kanıta Dayalı Tıp Yaklaşımı: Belirti ve Bulgulara Göre Tanı Olasılığını Hesaplamak
Tanı Olasılığını hesaplamak için Bayes teoremi (LR) Değerlerinden Yararlanılmıştır.
Parkinson hastalığı (PH) tanısı, tek başına hiçbir belirtinin yeterli duyarlılığa (Sen.) ve özgüllüğe (Spe.) sahip olmaması nedeniyle, temel olarak klinik gözlem ve MDS-UPDRS gibi standardize ölçeklerle konur. Tanısal süreçte, bir hekimin Bayes Teoremi'ni kullanarak ön olasılığı (prior) ve her yeni bulgunun LR değerini nasıl kullandığını detaylıca analiz ediyorum.
Parkinson Tanısı: Bayes Mantık ve LR Değerleri
2.1. Tanısal Kriterlerin Özü
PH'nin klinik tanısı, temel olarak hareket bozuklukları üzerine yoğunlaşır. Halen en yaygın kullanılan ve kabul gören kriterler, Uluslararası Hareket Bozuklukları Topluluğu (MDS) tarafından güncellenen kriterlerdir.
A. Gerekli Temel Kriter (Tanı Koymak İçin Zorunlu)
Bradikinezi: Hareketlerin yavaşlaması ve hızla tekrar eden hareketlerin amplitüdünün/hızının azalması (Örn: Parmak vuruşu). Bu, PH tanısı için mutlak zorunlu bir kriterdir.
B. Destekleyici Kriterler (Bradikinezi Yanında Olması Gerekenler)
Bradikinezi ile birlikte aşağıdaki majör semptomlardan en az birinin bulunması gerekir:
İstirahat Tremoru: İstirahatte belirgin, genellikle tek taraflı başlayan titreme.
Rijidite: Eklem hareketlerine karşı pasif direnç.
C. Mutlak Dışlama Kriterleri
Aşağıdaki durumların varlığı, PH tanısının kesinlikle dışlanmasını gerektirir (Başka bir Parkinsonizm sendromuna işaret eder):
Erken ve şiddetli bilişsel bozulma.
Erken dönemde serebellar bulgular (koordinasyon bozukluğu).
Göz hareketlerinin paralizi.
2.2. Temel Belirtilerin Tanı değerleri
Bu değerler, farklı çalışmalardan elde edilen ortalamaları yansıtır ve klinik akıl yürütmede kullanılır:
Belirti/Bulgu Duyarlılık (Sen) Özgüllük (Spe) LR+ LR−
Bradikinezi (Var olma) Yüksek ( 95%) Düşük-Orta (60%) 2.4 0.08
İstirahat Tremoru (Var olma) Orta ( 70%) Yüksek (85%) 4.7 0.35
Asimetrik Başlangıç Yüksek ( 80%) Yüksek (80%) 4.0 0.25
L-Dopa'ya Güçlü Yanıt Yüksek ( 90%) Yüksek (90%) 9.0 0.11
İdiopatik RBD (Prodromal) Düşük (30%) Çok Yüksek (95%) 6.0 0.73
Yorum:
LR+ Gücü: En yüksek LR+ değerine sahip bulgu, L-Dopa'ya güçlü yanıttır (LR+ 9.0). Bu bulgunun varlığı, PH olasılığını güçlü bir şekilde artırır.
LR− Gücü: Bradikinezinin olmaması, PH olasılığını güçlü bir şekilde azaltır (LR− 0.08)
2.3. Bayes Teoremi ve Ön Olasılığın Güncellenmesi
Doktorun akıl yürütmesini simüle eden A-DTA algoritmaları, başlangıçtaki ön olasılığı (P(H)) bilinen risk faktörleri ve LR değerleri ile günceller.
A. Ön Olasılığın Belirlenmesi (Prior)
PH'nin ön olasılığı, popülasyon verilerine ve bilinen risk faktörlerine göre başlar:
Yaş: PH prevalansı, yaşla birlikte üstel olarak artar. (Örneğin, 40 yaş altında düşük, 60 yaş üstünde yüksek başlangıç olasılığı).
Cinsiyet: Erkeklerde PH geliştirme riski, kadınlara göre 1.5 - 2.0 kat daha yüksektir.
Örnek Ön Olasılık Ayarı: 75 yaşındaki bir erkek hasta için, 60 yaşındaki bir kadına göre PH başlangıç olasılığı (P{H)) zaten daha yüksektir. Algoritma bu farkı başlangıçta sisteme yükler.
B. LR Değerleri ile Güncelleme Örneği
75 yaşındaki bir erkek hastada (Yüksek Ön Olasılık):
AdımKlinik Gözlem (Kanıt)LR DeğeriEtki
1.Koku Kaybı (Anosmi) (Prodromal) LR+ 2.0 Hastalığa olasılığını hafifçe artırır (Çarpım)
2.İstirahat Tremoru ve Bradikinezi Var. LR+ 4.7 Olasılığı güçlü bir şekilde artırır.
3.L}-Dopa'ya Güçlü Yanıt Var. LR+ 9.0 Olasılığı kesin tanıya çok yaklaştırır.
Matematiksel Mantık: Her LR değeri, hastalığın Odds Ratio'suyla çarpılır. L-Dopa'nın LR+ 9.0 olması, önceki tüm bulgularla birleştiğinde PH olasılığını klinik karar eşiğine (genellikle %90-%95)'e kadar çıkarır.
2.4. Klinik ve Laboratuvar Verilerinin Entegrasyonu
Tanıyı kesinleştirmek için klinik bulguların laboratuvar verileriyle desteklenmesi kritik öneme sahiptir.
A. Değerli Laboratuvar Verileri
DAT Tarayıcı (DaTScan): Bu görüntüleme testi, dopamin taşıyıcı yoğunluğunu ölçer. DaTScan'in normal çıkması, PH tanısını güçlü bir şekilde dışlar (LR− düşük), özellikle tremorun Esansiyel Tremor gibi PH dışı nedenlerden kaynaklandığı şüphesinde çok değerlidir.
Klinik Biyobelirteçler: Biyobelirteçler, özellikle Alfa-sinüklein Seed Assay gibi testler, PH için oldukça özgül olan Alfa-sinüklein topaklanmasını erken evrede saptayarak tanının kesinliğini (özgüllüğünü) artırma potansiyeline sahiptir.
B. Ayırıcı Tanı ve Dışlama
A-DTA algoritması, özellikle Atipik Parkinsonizm Sendromları'nı (MSA, PSP) dışlamak için klinik kriterlere başvurur. Bu sendromlarda genellikle L-Dopa'ya yanıt zayıftır (LR− zayıf), bu da PH olasılığını azaltır.
Bu bütünsel yaklaşım, doktorun sezgisel klinik deneyimini, ölçülebilir $\text{LR}$ değerleri ve olasılık matematiği ile güçlendirerek tanısal kesinliği artırır.
3. MEVCUT TIBBİ YAKLAŞIMLAR: DOPAMİN EKSİKLİĞİNİN TELAFİSİ
Ölen hücreleri canlandırmak henüz tam olarak mümkün olmasa da, modern ilaçlar semptomları güçlü bir şekilde yönetir.
Levodopa (L-Dopa), Altın Standart: Dopaminin öncülüdür, beyin bariyerini geçer ve dopamin'e dönüşür. Periferde yıkımını engelleyen dekarboksilaz inhibitörü ile kombine edilir. En güçlü semptomatik etkiyi sağlar, ancak uzun dönemde diskinezi gelişebilir.
Dopamin Agonistleri: Doğrudan dopamin reseptörlerini uyararak beynin dopamin almış gibi hissetmesini sağlar. Erken evrede veya L- Dopa ile kombine kullanılır. (Yan etki olarak dürtü kontrol bozukluğu olabilir. )
MAO-B / COMT İnhibitörleri: MAO-B inhibitörleri Monoamin Oksidaz-B) dopamin yıkımını azaltır; COMT inhibitörleri ise{L- Dopa'nın yıkımını azaltarak etki süresini uzatır (wear off döneminde yararlı).
"Wear-off" dönemi, Parkinson hastalığı (PH) tedavisinde sıklıkla karşılaşılan ve hastaların yaşam kalitesini ciddi şekilde etkileyen önemli bir klinik durumdur. Bu terim, özellikle Levodopa (L-Dopa) gibi dopamin replasman tedavilerinin etkisinin doz aralığı bitmeden, yani bir sonraki doz alınmadan hemen önce azalmasını ifade eder.
"Wear-off" döneminin tanımı, nedenleri ve etkileri:
"Wear-off" (etkinin aşınması/tükenmesi) terimi, Parkinson hastalığı olan bir hastanın motor semptomlarının, aldığı Levodopa ilacının bir sonraki dozu gelmeden önce yeniden kötüleşmesi durumunu tanımlar.
A. Mekanizma: Dopamin Depolarının Tükenmesi
Hastalığın erken evrelerinde, Substantia Nigra bölgesinde hala yeterince dopamin depolayan nöron bulunur. Bu nöronlar, L-Dopa'yı depolar ve gün boyunca istikrarlı bir şekilde salar.
Ancak hastalık ilerledikçe:
Dopamin Depolayan Nöron Kaybı Artar: Beyin, L-Dopa'yı alıp dopamin olarak depolayacak ve salıverecek çok az hücreye sahip kalır.
Etki Süresi Kısalır: İlaç alınınca L-Dopa kana karışır, beyne ulaşır ve dopamin'e çevrilir. Ancak bu yeni oluşan dopamin hızla kullanılır. Depo azaldığı için, ilacın kan seviyesi düşer düşmez, nöronlar yeterli dopamin sinyali alamaz.
Hızlı Geçiş: Hasta, ilacın etkili olduğu "Açık" (On) durumundan, semptomların geri döndüğü "Kapalı" (Off) duruma daha hızlı geçer.
B. Klinik Belirtileri
Wear-off döneminde, hastalar sıklıkla şu belirtilerin geri geldiğini veya kötüleştiğini hissederler:
Motor: Titreme (Tremor), hareketlerde yavaşlama (Bradikinezi), kas sertliği (Rijidite) ve yürüme güçlüğü.
Non-Motor: Anksiyete (kaygı), panik atak, ağrı, terleme ve duygusal değişimler de ortaya çıkabilir.
C. Yönetimi
Wear-off, PH tedavisinin ilerleyen aşamalarında sıkça görülür ve tedavinin temel amacı, hastanın "Açık" durumda geçirdiği süreyi uzatmaktır. Bu genellikle şu yollarla yapılır:
Doz Sıklığını Artırma: Aynı miktarda ilacı daha sık aralıklarla, daha küçük dozlarda vermek.
İlaç Kombinasyonu: L-Dopa'yı yıkan enzimleri (MAO-B veya COMT inhibitörleri) bloke eden ilaçları ekleyerek dopaminin ömrünü uzatmak.
Gelişmiş Tedaviler: İleri aşamalarda sürekli ilaç salınımı sağlayan infüzyon sistemleri veya DBS (Derin Beyin Stimülasyonu) uygulamak. Gelişmiş SistemlerDerin Beyin Stimülasyonu (DBS) veya infüzyon sistemleri}$ (Apomorfin/intestinal levodopa jel) gibi cerrahi veya sürekli ilaç verme yöntemleri, motor dalgalanmaları düzleştirmeyi hedefler.
4. GELECEK VİZYONU: REJENERASYON BİYOLOJİSİ
PH tedavisinde nihai hedef, hasar gören dopamin nöronlarını geri getirmektir.
Kök Hücre Temelli Yaklaşım: Dopaminerjik nöronlara farklılaşabilen indüklenmiş Pluripotent Kök Hücrelerin (PSC) Substantia Nigra'ya nakledilmesi üzerine yoğun çalışmalar sürmektedir. Zorluklar arasında bağışıklık yanıtı, tümörleşme riski ve doğru sinir ağı bağlantılarının kurulması yer alır.
Nörotrofik Destek ve Gen Düzenleme: GDNF veya BDNF gibi nörotrofik faktörlerin gen transferi yoluyla artırılması, dopamin nöronlarının sağkalımını ve filizlenmesini destekleyebilir.
5. FİTOTERAPİ VE METABOLİTLER: DOLAYLI NÖROPROTEKSİYON
Bitkisel bileşenler ve metabolitler, modern tedavinin bıraktığı boşlukları doldurarak nöroinflamasyonu ve oksidatif stresi yönetir. Kanıt durumları heterojendir ve klinik kullanımdan önce hekim danışmanlığı şarttır.
A. Doğrudan Dopamin Kaynağı ve Puanı
Mucuna Pruriens: Doğrudan ve doğal L-Dopa içerir. Dopamin eksikliğini doğrudan hedefleyen en güçlü bitkisel adaydır. Modern L-Dopa'ya benzer semptomatik etki sağlar, ancak standardizasyon ve ilaç etkileşim riski nedeniyle tıbbi izlem zorunludur.
B. Nöroprotektif Mekanizmaların Analizi
TUDCA (Tauroursodeoxycholic acid):
Etki Mekanizması: Mitokondri ve ER Stres Azaltımı
Nörolojik Rejenerasyonda Rolü: PH patogenezinde rol oynayan endoplazmik retikulum (ER) stresini azaltarak Lewy Cisimciği oluşumunu dolaylı olarak baskılar.
Fisetin:
Etki Mekanizması: Senolitik ve Antioksidan
Nörolojik Rejenerasyonda Rolü: Nöronal hasara katkıda bulunan yaşlanmış hücreleri temizler; nöroinflamasyonu azaltır ve nöron sağkalımını destekler.
Rhodiola Rosea:
Etki Mekanizması: Adaptojenik ve Mitokondriyal Destek
Nörolojik Rejenerasyonda Rolü: Stres hormonları (kortizol) üzerindeki baskıyı azaltır. Mitokondriyal disfonksiyonu ve ATP düşüşünü dengeleyerek nöronların dayanıklılığını artırır.
Berberin:
Etki Mekanizması: AMPK Aktivasyonu
Nörolojik Rejenerasyonda Rolü: Hücresel enerji metabolizmasını düzenler ve nöroinflamasyonu azaltır. Beyin–bağırsak ekseni modülasyonuna katkıda bulunur.
Sitikolin (CDP Kolin):
Etki Mekanizması: Nöron Zarı Bütünlüğü
Nörolojik Rejenerasyonda Rolü: Nöron zarı bileşeni olan fosfolipit sentezini destekler. Nöron hasarı sonrası hücre zarı onarımı için kritik hammadde sağlar.
Vitamin D3:
Etki Mekanizması: Nöroimmün Modülasyon
Nörolojik Rejenerasyonda Rolü: Nöroprotektif etkilere sahiptir; düşük D vitamini seviyeleri, kötü PH prognozuyla ilişkilendirilmiştir. Eksikliğin düzeltilmesi zorunludur.
Gastrodia (Tian Ma):
Etki Mekanizması: Geleneksel Dopamin Desteği
Nörolojik Rejenerasyonda Rolü: Nöroinflamasyon ve oksidatif stresi azaltır; geleneksel olarak tremor semptomlarını hafifletmek için kullanılmıştır.
C. Geleneksel Çin Tıbbı ve Diğer Destekler
Epimedium (ikarin), Ellagic asit (Nar), Bacopa monnieri, Pregnenolon ve L-Dopa (ilaç formatında) gibi bileşenler; antioksidan, anti-inflamatuar ve nörotrofik destekleri ile dopamin nöronlarının sağkalımını destekleyen geniş bir spektrum sunar.
Sonuç: Parkinson tedavisi, güçlü semptom kontrolü (L-Dopa) ile nöron sağkalımı ve rejeneratif biyoloji arasındaki sinerjiyi kurmaya odaklanmalıdır. Gelecekteki klinik yol haritası, Fisetin gibi temizleyici ajanlarla hasarlı ortamı hazırlamak ve kök hücre/nörotrofik yaklaşımlarla hasarlı nöronları yerine koymaktır.