" Bilim. Kanıt. Şifa. | Dr. Aleksi: Yeni Nesil Sağlık Ekosistemi."
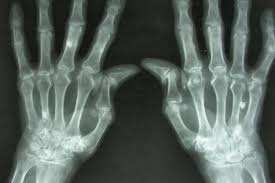
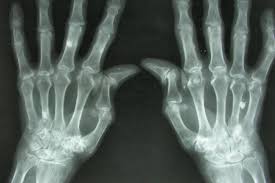
ROMATOİD ARTRİT: BEDENİN KENDİNE AÇTIĞI SAVAŞIN HİKÂYESİ
KAS VE İSKELET SİSTEMİHASTALIK & SENDROMKRONİK HASTALIKLARARTROPATİ & ROMATALJİ
Dr. Aleksi
12/16/20257 min oku
ROMATOİD ARTRİT: BEDENİN KENDİNE AÇTIĞI SAVAŞIN HİKÂYESİ
Bu, mikroskobik düzeyde başlayan bir yanlış anlaşılmanın, eklemlerdeki yıkıcı bir fırtınaya dönüşmesinin epik hikâyesidir. Modern tıp merceğinden baktığımızda Romatoid Artrit (RA), sadece bir "eklem ağrısı" değil, bağışıklık sisteminin kendi dokusunu yabancı bir işgalci sanarak başlattığı çok katmanlı bir kuşatmadır.
1. Bölüm: Karmaşanın Başlangıcı (Etiyopatogenez)
Her şey sessizce başlar. Genetik kodumuzdaki HLA-DRB1 ("shared epitope") gibi bariz olmayan bir yatkınlık, çevresel bir tetikleyiciyle buluşur. Bu bazen bir sigara dumanındaki toksin, bazen diş etindeki bir bakteri (Porphyromonas gingivalis), bazen de bağırsak mikrobiyotasındaki küçük bir değişimdir.
Vücut, proteinleri "sitrülinasyon" adı verilen bir işlemle modifiye ederken, bağışıklık sisteminin gözcüleri olan T ve B hücreleri bu yerli proteinleri düşman ilan eder. Anti-CCP (ACPA) ve RF adı verilen "ihanet mektupları" (otoantikorlar) kan dolaşımına salınır. Bu, biyolojik bir iç savaşın ilanıdır.
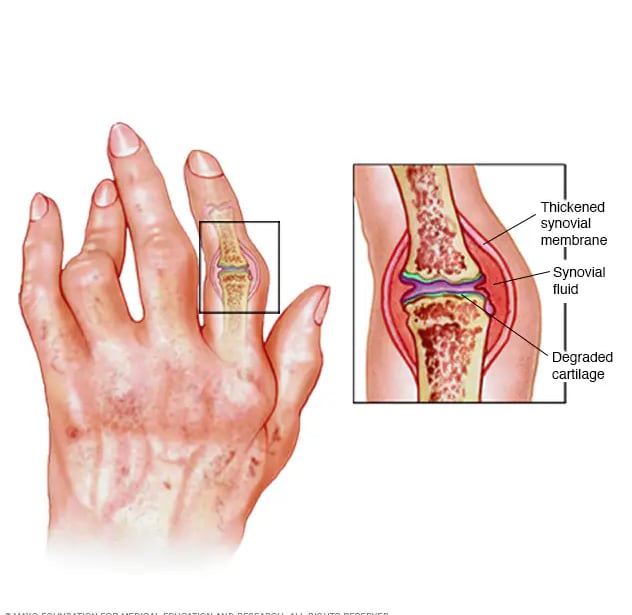
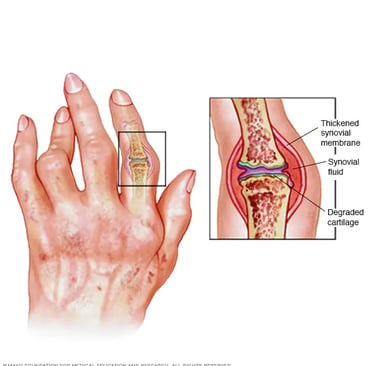
2. Bölüm: Kuşatma Altındaki Kale (Sinovyum ve Pannus)
Normalde ince ve şeffaf olan eklem zarı (sinovyum), bu saldırı altında hızla kalınlaşmaya başlar. Damarlar kontrolsüzce çoğalır ve pannus adı verilen, saldırgan bir doku oluşur. Bu doku, adeta bir asit gibi kıkırdağı eritir ve kemiği kemirir. TNF-α, IL-1 ve IL-6 gibi sitokinler, yangını körükleyen moleküler yakıtlardır. Sonuç; sabahları kilitlenen, şişmiş ve yavaş yavaş şekil değiştiren eklemlerdir.
3. Bölüm: Teşhisin Matematiği ve Bayesçi Dedektiflik
Bir hastanın kliniğe girişiyle birlikte, hekim bir Bayesçi olasılık hesabı yapmaya başlar. Başlangıçta RA şüphesi bir "prior" (ön olasılık) olarak %20-30 düzeyindedir. Şimdi, her yeni veri bu olasılığı nasıl güncelliyor, görelim:
Simetrik Küçük Eklem Tutulumu: Sens. %60 - 80 Spe. %70 - 90 LR(+) ~3 -5. Olasılığı orta derecede artırır. Sabah Tutukluğu (>1 Saat): Sens. %75 - 85, Spe. %30 - 40 LR(+) ~1.5 Spesifik değildir ama varlığı değerlidir. Anti-CCP (ACPA): Sens. %67 - 80 Spe. %95 - 98 LR(+) 12 - 20 En güçlü kanıt. Olasılığı %90 üzerine taşır. Romatoid Faktör (RF): Sens. %60 - 70 Spe. %70 - 85 LR(+) 3 - 5. Destekleyicidir ancak tek başına yetersizdir. Erozyon (Radyografi): Sens. %45 - 50 Spe. %90 - 95 LR(+) ~8 Geç kalındığını ama tanının netliğini gösterir.
Ayırıcı Tanıda Farklılıklar:
Osteoartrit: Sabah tutukluğu 30 dakikadan azdır, CRP normaldir, erozyon yoktur.
Psöriyatik Artrit: Asimetriktir, tırnaklarda çukurlaşma ("pitting") ve "daktilit" (sosis parmak) görülür.
Sistemik Lupus (SLE): Artrit eroziv değildir (eklemi yıkmaz), Anti-dsDNA pozitiftir.
4. Bölüm: Karşı Saldırı (Tedavi Stratejileri)
Modern tıp, "Pencere Dönemi"ni (ilk 3-6 ay) kaçırmamayı hedefler. Strateji: Treat-to-Target (Hedefe Yönelik Tedavi).
Geleneksel DMARD'lar: Metotreksat, bağışıklık sisteminin aşırı hızını kesen "fren" sistemidir.
Biyolojik Ajanlar: Anti-TNF (Adalimumab) veya Anti-IL-6 (Tocilizumab), savaşın ana generallerini (sitokinleri) hedef alan akıllı füzelerdir.
JAK İnhibitörleri: Hücre içindeki sinyal iletim yollarını keserek haberleşmeyi durdurur.
Klinik pratikte devrim yaratan Anti-TNF (Tümör Nekroz Faktör) İnhibitörleri ve onların yeni nesil rakipleri olan JAK İnhibitörlerini (Janus Kinaz) mercek altına alalım.
Bu analizde, bu ilaçların neden "akıllı" olduğunu, hücrenin içinde ve dışında hangi kaleleri zapt ettiklerini ve en önemlisi "Neden bir hastada biri çalışırken diğerinde diğeri çalışıyor?" sorusunun arkasındaki moleküler mekanizmayı inceleyeceğiz.
Moleküler Düellonun Perde Arkası: Anti-TNF vs. JAK İnhibitörleri
RA tedavisindeki bu iki dev gücü bir belgesel kamerasıyla izleyelim:
1. Anti-TNF Ajanlar: "Hücre Dışı Diplomasinin Sonu"
Anti-TNF'ler (Adalimumab, Infliximab, Etanercept), savaş alanındaki (sinovyal sıvı) ana saldırgan olan TNF-alpha molekülünü yakalayan "moleküler ağlar" gibidir.
Mekanizma: TNF-alpha, bağışıklık sisteminin en güçlü yangın başlatıcısıdır. Anti-TNF'ler, bu molekülün kendi reseptörüne bağlanmasını engeller. Bu sayede endotel hücrelerinden adezyon molekülleri salınmaz, lökositler ekleme akın edemez.
Klinik Kanıt: ASPIRE ve PREMIER gibi dönüm noktası çalışmalar, Anti-TNF + Metotreksat kombinasyonunun, tek başına tedaviye göre radyolojik progresyonu (kemik yıkımını) dramatik şekilde durdurduğunu kanıtlamıştır.
Bayesçi Bakış: Eğer bir hastada CRP/ESR çok yüksekse ve sistemik inflamasyon baskınsa, Anti-TNF'lerin "temizleme" kapasitesi (LR+) oldukça yüksektir.
2. JAK İnhibitörleri: "Hücre İçi Haberleşme Sabotajı"
JAK inhibitörleri (Tofacitinib, Upadacitinib) biyolojik ilaç değildir; "küçük moleküllü" ilaçlardır. Bunlar hücrenin içine girer ve JAK-STAT sinyal yolunu bloke ederler.
Mekanizma: Bir sitokin hücrenin kapısını (reseptörünü) çaldığında, mesajı çekirdeğe ileten bir "postacı" (JAK enzimi) gerekir. JAK inhibitörleri bu postacıyı durdurur.
Önemli Fark: Anti-TNF sadece tek bir molekülü (TNF) durdururken, bir JAK inhibitörü aynı anda IL-2, IL-6, IL-12, IL-15, IL-21 ve İnterferon-gamma gibi birçok farklı saldırganın mesajını engelleyebilir.
Klinik Kanıt: ORAL Strategy ve SELECT çalışmaları, JAK inhibitörlerinin biyolojik ajanlara yanıt vermeyen dirençli vakalarda bile yüksek remisyon oranları sağladığını göstermiştir.
Karşılaştırmalı Analiz Tablosu
Anti-TNF (Biyolojikler):
Hedef: Hücre dışı (Sitokinin kendisi)
Uygulama: Enjeksiyon veya İnfüzyon
Yarı Ömür: Uzun (Günler/Haftalar)
İmmünojenite: İlaç karşıtı antikor gelişebilir
En Büyük Risk: Tüberküloz reaktivasyonu
JAK İnhibitörleri (Küçük Moleküller)
Hedef: Hücre içi (Sinyal iletim yolu)
Uygulama. Oral (Hap)
Yarı Ömür: Kısa (Saatler)
İmmünojenite:Antikor gelişme riski yoktur
En Büyük Risk: Herpes Zoster (Zona) riski, Tromboemboli
"Hangi İlaç, Hangi Hastaya?" (Klinik Karar Verme)
Burada devreye Kişiselleştirilmiş Tıp giriyor. Bir hastaya hangi silahla saldıracağımızı seçerken şu fenotiplere bakıyoruz:
Hızlı Etki Gerekiyorsa: JAK inhibitörleri, kısa yarı ömürleri ve oral emilimleri sayesinde genellikle gün/hafta bazında daha hızlı klinik yanıt (ağrıda azalma) verebilir.
Kardiyovasküler Risk Varsa: JAK inhibitörlerinde tromboz riski (özellikle 65 yaş üstü ve sigara içenlerde) daha dikkatli yönetilmelidir. Bu durumda Anti-TNF'ler daha güvenli bir liman olabilir.
İğne Korkusu/Uyum Sorunu: Oral tedavi (JAK-i), hasta uyumunu (compliance) %30-40 oranında artırabilmektedir.
Tüberküloz Endemik Bölge: Anti-TNF kullanımı öncesi latent TB taraması hayati önem taşır; JAK inhibitörlerinde de risk vardır ancak yönetimi farklılık gösterir.
Gelecek, Biyobelirteç Odaklı tedavide. Yakında bir hastanın sinovyal doku biyopsisini yaparak; "Bu hastanın pannusunda IL-6 baskın, o halde Tocilizumab verelim" veya "Burada JAK-STAT yolu hiperaktif, doğrudan Tofacitinib ile başlayalım" diyebileceğiz.
Refrakter RA: Kurtarma Protokolleri (Rescue Therapy)
Standart tedavilere yanıt vermeyen bir hastada, "moleküler bir değişim" gerekir. İşte en güçlü stratejiler:
1. B-Hücre Deplesyonu (Rituksimab Stratejisi)
Eğer sitokin inhibitörleri (Anti-TNF, JAK-i) başarısız olduysa, sorun sitokinlerin kendisinden ziyade, onları sürekli üreten fabrikalarda olabilir.
Mekanizma: Rituksimab, B-lenfositlerin üzerindeki CD20 molekülüne bağlanarak bu hücreleri ortadan kaldırır. "Fabrikayı kapatarak" antijen sunumunu ve otoantikor (RF/ACPA) üretimini durdurur.
Klinik İpucu: RF ve Anti-CCP değerleri çok yüksek (seropozitif) olan hastalarda Rituksimab'ın başarı şansı (LR+), seronegatif hastalara göre anlamlı derecede daha yüksektir.
2. T-Hücre Kostimülasyon Blokajı (Abatacept Stratejisi)
Bağışıklık sisteminin "generalleri" olan T-hücreleri, aktive olmak için iki farklı sinyale (el sıkışmasına) ihtiyaç duyar.
Mekanizma: Abatacept (CTLA-4 Ig), bu el sıkışmasını (CD80/86 ve CD28 etkileşimi) engeller. T-hücresi aktive olamazsa, tüm inflamatuar kaskad daha en başında "uyku moduna" geçer.
Avantajı: Özellikle akciğer tutulumu (Interstisyel Akciğer Hastalığı) olan RA vakalarında daha güvenli bir profil sergilediği düşünülmektedir.
3. "Cycling" (Döngü) vs. "Switching" (Değiştirme)
Klinik karar verme noktasında iki yol vardır:
Cycling: Bir Anti-TNF başarısız olduğunda başka bir Anti-TNF'ye geçmek. (Genellikle ilaç karşıtı antikor gelişen vakalarda tercih edilir).
Switching: Etki mekanizmasını tamamen değiştirmek (Örn: Anti-TNF'den JAK inhibitörüne veya IL-6 inhibitörüne geçmek). Refrakter vakalarda Switching, genellikle daha yüksek yanıt oranları (ACR50/70 yanıtı) sağlar.
Tedavi Direncini Analiz Etmek: Neden Cevap Alamıyoruz?
Kurtarma protokolüne geçmeden önce, direncin "yalancı" olup olmadığını anlamalıyız:
Non Adherence (Uyumsuzluk): Hastanın ilacı gerçekten kullanıp kullanmadığı sorgulanmalı (Özellikle oral JAK-i).
İkincil Fibromiyalji: Hasta ağrı tanımlıyor ama CRP/ESR normal mi? Ağrının kaynağı inflamasyon olmayabilir.
İmmünojenite: Biyolojik ilaca karşı antikor gelişmiş olabilir. (İlaç düzeyi takibi gerekebilir).
Yanlış Fenotip: Hasta aslında Psöriyatik Artrit veya Spondiloartrit mi?
Geleceğin Kurtarma Protokolü: "Synovial Biopsy-Driven" Tedavi
Artık deneme-yanılma yönteminden uzaklaşıyoruz. R4RA Çalışması gibi güncel araştırmalar gösteriyor ki; sinovyal dokuda B-hücresi az olan bir hastaya Rituksimab vermek zaman kaybıdır. Gelecekte hastanın ekleminden alınan küçük bir parça (ultrason eşliğinde biyopsi) ile hangi yolağın baskın olduğunu saptayıp, nokta atışı tedavi (Precision Medicine) seçeceğiz.
Prognozda "Zorunlu" Hedef: Remisyon
Refrakter vakalarda bile hedefimiz artık "biraz iyileşme" değil, DAS28 < 2.6 (Remisyon) veya en azından düşük hastalık aktivitesidir. Çünkü her geçen gün süren inflamasyon, sadece eklemi değil, vasküler endoteli de bozarak kardiyovasküler riski (MI/İnme) artırır.
5. Bölüm: Doğanın Eczanesi (Moleküler Metabolitler)
Bilimsel literatürde (özellikle in-vitro ve hayvan modellerinde) RA'nın inflamatuar yolaklarını baskıladığı kanıtlanmış 7 temel metabolit:
Kurkumin (Zerdeçal): NF-κB yolağını bloke ederek sitokin fırtınasını dindirir.
Boswellik Asit: 5-LOX enzimini inhibe ederek lökotrien sentezini (iltihap habercileri) durdurur.
Resveratrol: Sirtuin-1 aktivasyonu üzerinden sinovyal hücrelerin kontrolsüz çoğalmasını (pannus oluşumunu) yavaşlatır.
EGCG (Yeşil Çay): Kemik yıkımından sorumlu olan osteoklastların aktivitesini baskılar.
Gingerol (Zencefil): Hem COX hem de LOX yolaklarını aynı anda etkileyen doğal bir dual inhibitör gibidir.
Quercetin: Mast hücrelerini stabilize ederek ve TNF-α salınımını azaltarak sistemik yükü hafifletir.
Omega-3 (EPA/DHA): Hücre zarındaki araşidonik asit ile yarışarak pro-inflamatuar eikosanoidlerin üretimini azaltır.
Sonuç ve Prognoz
Romatoid Artrit, tedavi edilmediğinde 10 yıl içinde hastaların yarısını maluliyetle karşı karşıya bırakan bir dramdır. Ancak bugünkü Bayesçi tanı hızı ve biyolojik silahlarımızla, bu dramın sonunu değiştirmek bizim elimizdedir. Erken müdahale, sadece eklemleri değil, bir hayatın hareket kabiliyetini kurtarır.