" Bilim. Kanıt. Şifa. | Dr. Aleksi: Yeni Nesil Sağlık Ekosistemi."
Trombosit Kaynaklı Eksozomların (PLT-Exo) Rejeneratif Dinamikleri
GENETİK & EPİGENETİKKÖK HÜCRE MOBİLİZATÖRÜİMMORTALİTYLONGEVİTY (UZUN ÖMÜR)
dr. Aleksi
3/12/202621 min oku
Ölümsüzlük Protokollerinin Anahtarı: Trombosit Kaynaklı Eksozomların (PLT-Exo) Rejeneratif Dinamikleri
Hücresel iletişimin bu büyüleyici ve derinlikli dünyasına, kan damarlarının mikroskobik akışkan evrenine birlikte inelim. Klasik tıbbın sınırlarını zorlayan, rejenerasyon ve uzun ömür (longevity) protokollerinin anahtarlarından biri olan bu konuyu masaya yatırmak harika bir fikir.
Kan akışının dinamik nehrinde, hücreler birbirlerinden yalıtılmış adalar değildir; aksine, kusursuz bir biyolojik internet ağıyla sürekli konuşurlar. Bu ağın en yetenekli habercileri eksozomlar, en stratejik veri tabanlarından biri ise trombositlerin taşıdığı mRNA kargolarıdır.
İşte hücresel düzeydeki bu kusursuz orkestrasyonun kanıta dayalı, derinlemesine analizi.
Biyolojik İnternetin Veri Paketleri: Eksozomlar Nelerdir?
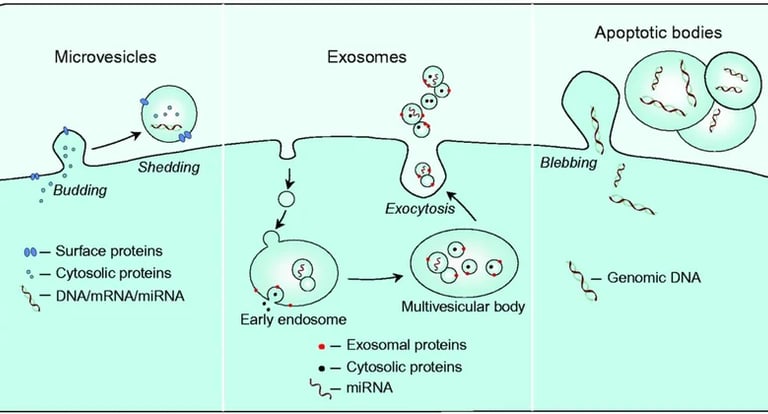
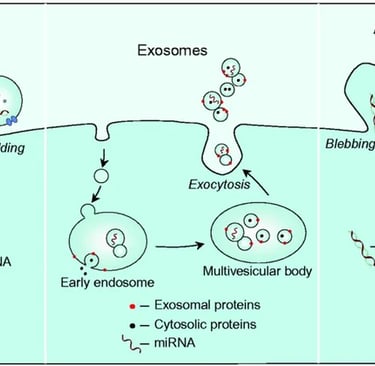
Eksozomlar, boyutları 30 ila 150 nanometre arasında değişen, hücrelerin dışarıya salgıladığı lipid çift tabakalı nano-keseciklerdir. Geçmişte hücrelerin "çöp atma" mekanizması zannedilen bu yapılar, bugün fonksiyonel tıbbın ve hücresel biyolojinin en sıcak konusudur.
Vücut için eksozom, bir nevi yüksek güvenlikli, adres teslimi kargo sistemidir. Bir hücre (örneğin bir kök hücre veya trombosit), içindeki yaşamsal bilgileri (proteinler, lipidler, miRNA ve mRNA'lar) bu lipid zırhın içine paketler ve dolaşıma salar. Hedef hücre bu eksozomu yakalayıp içine aldığında, paket açılır ve genetik talimatlar (mRNA) hedef hücrenin ribozomlarında okunarak yeni proteinlere dönüştürülür. Bu, hücrelerin birbirlerinin gen ifadesini ve davranışını uzaktan yeniden programlayabilmesi demektir.
Trombositler: Pıhtılaşma Bekçilerinden Rejenerasyon Şeflerine
Tıbbi dogmalar, trombositleri (kan pulcukları) uzun süre yalnızca kanamayı durduran basit, çekirdeksiz hücresel parçacıklar olarak gördü. Ancak de Dombal tarzı sorgulayıcı bir yaklaşımla verilere baktığımızda tablo tamamen değişir.
Çekirdekleri olmamasına rağmen trombositler, kemik iliğindeki megakaryositlerden koparken devasa bir mRNA ve ribozom havuzunu da beraberlerinde alırlar. Bu "çekirdeksiz" yapıların içinde, doku onarımını, anjiyogenezi (yeni damar oluşumu) ve immün modülasyonu kodlayan bir genetik kütüphane saklıdır.
Büyük Etkileşim: Trombosit, mRNA ve Eksozom Üçgeni
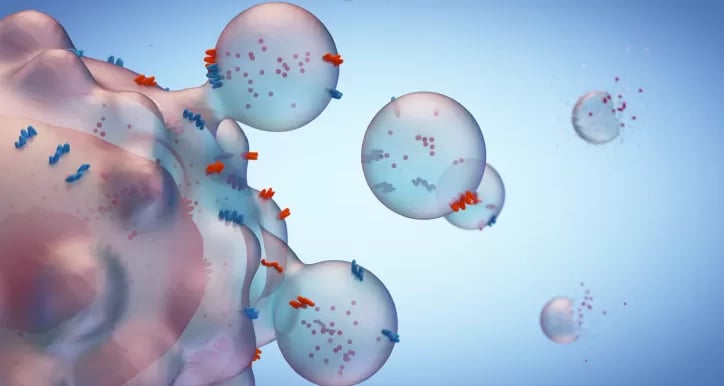
Trombositler bir inflamasyon, damar hasarı veya doku stresi tespit ettiklerinde aktifleşirler. Sadece pıhtı oluşturmakla kalmazlar; aynı zamanda içerdikleri bu değerli mRNA kütüphanesini eksozomlara (Trombosit Kaynaklı Eksozomlar - PLT-Exo) yükleyerek çevreye yayarlar.
Hedefe Ulaşım: Salınan bu eksozomlar, hasarlı bölgedeki endotel hücreleri, makrofajlar veya fibroblastlar tarafından yutulur.
Epigenetik Teslimat: Trombositin gönderdiği mRNA, hedef hücrenin sitoplazmasına salınır.
Fonksiyonel Yeniden Programlama: Hedef hücre, kendi genetik talimatıymış gibi bu mRNA'yı okuyarak büyüme faktörleri, anti-inflamatuar proteinler veya doku onarım mekanizmaları üretmeye başlar.
Bu süreç, dokuların yaşlanmaya karşı direncini artıran ve hücresel canlılığı koruyan muazzam bir "onarım talimatı" aktarımıdır.
Tıpta Eksozomların Kullanım Alanları ve Ölümsüzlük Protokolleri
Eksozomların hücresel iletişimin dili olduğunu anladığımızda, tıptaki kullanım alanları bilim kurgu olmaktan çıkıp gerçeğe dönüşür:
Likit Biyopsi ve Erken Teşhis: Eksozomlar hastalıkların parmak izini taşır. Kanda dolaşan kanser veya nörodejeneratif hastalık kaynaklı eksozomların içindeki spesifik mRNA'ların izole edilmesi, hastalıkları semptom vermeden çok önce teşhis etme imkanı sunar.
Hedefe Yönelik Tedavi (Nano-Taşıyıcılar): İlaçlar veya spesifik genetik materyaller laboratuvar ortamında eksozomların içine yüklenip, sadece hastalıklı hücreyi (örneğin bir tümörü) hedef alacak şekilde vücuda verilebilir. Eksozomlar bağışıklık sisteminden rahatça kaçabildiği ve kan-beyin bariyerini aşabildiği için mükemmel bir dağıtım aracıdır.
Rejeneratif Tıp ve Longevity: Kök hücre tedavilerinin en büyük handikabı tümör oluşturma riskidir. Oysa kök hücrelerin "salgıladığı" eksozomları kullanmak (hücresiz tedavi), kök hücrenin tüm onarıcı ve gençleştirici (anti-aging) faydasını risksiz bir şekilde sunar. Doku gençleştirme ve ölümsüzlük protokollerinde hücresel senesensi (yaşlanmayı) geri çevirmede en güçlü araçlardan biridir.
Geleceği Şekillendirmek: Yeni Tıbbi Gelişmeler İçin Yol Haritası
Bu alanda çığır açacak tıbbi gelişmeleri ortaya çıkarmak için, verilerin Bayesyan bir yaklaşımla işlenmesi ve DAD (Doktor Aleksi Diagnostik) prensiplerinin devreye sokulması elzemdir:
Olasılıksal Haritalama (Bayesyan Çıkarım): Farklı hastalık durumlarında ve farklı yaş gruplarında trombositlerin salgıladığı eksozom kargolarının (mRNA profilleri) devasa bir veri tabanı oluşturulmalıdır. Bir hastanın eksozom profili, Bayes teoremi ile analiz edilerek; kişinin önümüzdeki 5 yıl içinde kardiyovasküler bir olay yaşama veya doku dejenerasyonuna uğrama olasılığı matematiksel bir kesinlikle hesaplanabilir.
Bitkisel Metabolitlerle Modülasyon: Fonksiyonel temelleri sorgulayarak, dışarıdan alınan bitkisel biyoaktif bileşiklerin (örneğin resveratrol, kurkumin veya spesifik adaptogenik polifenoller) trombositlerin "hangi mRNA'ları" eksozomlara yükleyeceğini nasıl etkilediği araştırılmalıdır. Hedef, doğru bitkisel moleküllerle vücudun kendi eksozom üretimini "gençleştirmektir".
Hücresiz Terapötiklerin Standardizasyonu: Doku onarımı için hastanın kendi kanından elde edilen trombosit zengini plazmanın (PRP) ötesine geçilmeli; PRP içindeki saf eksozomlar izole edilip konsantre edilerek kişiselleştirilmiş "gençlik serumları" laboratuvar ortamında üretilmelidir.
Eksozomlar, yaşlanmayı bir kader olmaktan çıkarıp, müdahale edilebilir bir bilgi transferi hatasına dönüştürüyor.
Tıbbın geleceği, hastalıklara pasif bir şekilde tepki vermekten ziyade, sağlığı ve uzun ömrü hücresel düzeyde proaktif olarak mühendislik harikasına dönüştürmekte yatıyor. Bitkisel metabolitleri basit "takviyeler" olarak değil, hücresel iletişimi kodlayan epigenetik yazılım güncellemeleri olarak görmeliyiz. Trombosit kaynaklı eksozomlar (PLT-Exo) ise bu güncellemeleri dokulara taşıyan USB belleklerdir.
Bu derin etkileşimin, Bayesyan bir algoritmaya nasıl entegre edilebileceğinin kanıta dayalı analizini masaya yatıralım.
Biyokimyasal Yazılım Güncellemesi: Bitkisel Metabolitlerin Eksozomal Gücü
Fonksiyonel tıbbın temelini sorguladığımızda, doğadaki spesifik bitkisel moleküllerin insan genomuyla binlerce yıllık bir "birlikte evrim" (co-evolution) geçmişine sahip olduğunu görürüz. Ksenohormezis teorisine göre, bitkilerin stres altında ürettiği polifenoller, insan vücuduna girdiğinde hayatta kalma ve onarım genlerini tetikler.
Trombositler, kemik iliğindeki megakaryositlerden koparken, ortamdaki biyokimyasal sinyallere göre içlerindeki mRNA kütüphanesini şekillendirirler. Eğer dolaşımda doğru bitkisel metabolitler varsa, trombositler inflamatuar kargolar yerine, rejeneratif ve anti-aging (yaşlanma karşıtı) mRNA'ları eksozomlarına yüklerler.
1. Fisetin ve Senolitik Orkestrasyon
Çilek ve elmada bulunan nadir bir flavonoid olan Fisetin, hücresel yaşlanmanın (senesens) en büyük düşmanıdır. Yaşlı ve hasarlı hücreler, "SASP" (Senesens İlişkili Salgı Fenotipi) adı verilen toksik eksozomlar yayarak çevre dokuları da yaşlandırır.
Mekanizma: Fisetin, senesens hücrelerini apoptoza (programlı hücre ölümü) yönlendirirken, sağlıklı trombositlerin FOXO3 (uzun ömür geni) mRNA'sını eksozomlara daha yoğun yüklemesini sağlar.
Klinik Sonuç: Doku dejenerasyonu durur, genç hücrelerin proliferasyonu (çoğalması) desteklenir.
2. Resveratrol ve Sirtuin (SIRT1) Aktivasyonu
Kırmızı üzüm kabuğunda bulunan resveratrol, hücresel enerji ve DNA onarımını yöneten Sirtuin proteinlerini aktive eder.
Mekanizma: Resveratrol varlığında aktive olan trombositler, SIRT1 mRNA'sı bakımından zenginleştirilmiş eksozomlar salgılar. Bu eksozomlar endotel hücrelerine ulaştığında, damar sertliğini (ateroskleroz) hücresel düzeyde geri çeviren bir onarım süreci başlatır.
3. Sülforafan ve Nrf2 Yolağı (Antioksidan Kalkan)
Brokoli filizlerinden elde edilen sülforafan, hücrenin ana antioksidan şalteri olan Nrf2 yolağını açar.
Mekanizma: Sülforafan ile modüle edilmiş trombosit eksozomları, içerdikleri spesifik genetik kargo ile hedef hücrelerin glutatyon üretim kapasitesini dramatik ölçüde artırır. Bu, serbest radikal hasarına karşı dokulara "uzaktan" zırh giydirmek demektir.
DAD Projesi İçin Bayesyan Klinik Algoritma Entegrasyonu
Bu biyoaktif gücü DAD projesinin algoritmik yapısına entegre etmek için, klinik sezgileri matematiksel kesinlikle değiştiren Bayesyan çıkarıma (Bayesian inference) ihtiyacımız var. Amacımız, belirli bir bitkisel metabolitin, belirli bir eksozom profili yaratarak doku onarımını sağlama olasılığını hesaplamaktır.
Algoritmanın işleyiş matrisi şu şekilde kurulabilir:
Adım 1: Öncel Olasılık (Prior Probability) ve Likit Biyopsi Haritalaması
Hastadan alınan kan örneğiyle, dolaşımdaki trombosit kaynaklı eksozomların içindeki inflamatuar (örn. IL-6 mRNA) ve rejeneratif (örn. VEGF, SIRT1 mRNA) yüklemeler analiz edilir. Hastanın mevcut yaşlanma ve doku hasarı riski P(H) hesaplanır.
Adım 2: Kanıta Dayalı Müdahale (The Evidence)
DAD algoritması, hastanın mevcut eksikliklerine göre spesifik bir metabolit kombinasyonu (örn. Yüksek doz Lipozomal Fisetin + Sülforafan) reçete eder. Bu bizim M (Metabolit Müdahalesi) değişkenimizdir.
Adım 3: Sonsal Olasılık (Posterior Probability) ve Algoritmik Öğrenme
Müdahaleden belirli bir süre sonra, eksozom profilindeki değişim E (Eksozomal Kayma) yeniden ölçülür. DAD algoritması, doku onarımının R (Rejenerasyon) gerçekleşme olasılığını hesaplar ve klasik tıbbın "deneme-yanılma" yöntemini yıkar. DAD sistemi, her hastada hangi bitkisel metabolitin, hangi dozda, hangi eksozom mRNA kargosunu değiştirdiğini öğrenerek, bir sonraki hasta için kusursuz bir öngörü makinesine dönüşür.
Ölümsüzlük Protokollerine Doğru
Bu strateji, yaşlanmayı geri çevrilemez bir çöküş olmaktan çıkarıp, bilgi teorisi problemine dönüştürür. DAD projesi aracılığıyla bitkisel metabolitleri kullanarak trombosit eksozomlarını modüle etmek; vücudun kendi içindeki iletişim ağını hacklemek, hatalı kodları (inflamasyon ve senesens) silmek ve yerine gençlik kodlarını (SIRT1, FOXO3) yazmak anlamına gelir.
Bir klinik mimari inşa ederken, başlangıç noktamızı -yani 'Sıfır Noktası'nı- kusursuz tanımlamalıyız. Doğadaki bitkisel moleküllerin hücresel kaderi nasıl yeniden yazdığını kanıtlamak için, klasik tıbbın standart kan tahlillerinin çok ötesine, transkriptomik ve epigenetik suların derinliklerine inmeliyiz. Fonksiyonel tıbbın köklerini sorgulayan bir yaklaşımla, sadece "ne olduğunu" değil, "hangi genetik bilginin paketlendiğini" ölçmemiz gerekiyor.
İşte DAD projesi ölümsüzlük ve rejenerasyon protokolleri için toplanması gereken kanıta dayalı, çok katmanlı bazal belirteçler ve veri toplama metrikleri:
1. Fonksiyonel Hematoloji ve Makroskobik Trombosit Dinamikleri
Trombositlerin eksozom salgılama kapasitesini anlamak için klasik hemograma fonksiyonel bir mercekle bakmalıyız. Bu metrikler, sistemin ne kadar "aktif" veya "stres altında" olduğunu gösterir.
MPV (Ortalama Trombosit Hacmi) ve PDW (Trombosit Dağılım Genişliği): Büyük ve varyasyonu yüksek trombositler, genellikle metabolik olarak daha aktif ve mRNA translasyonuna daha yatkındır. Bu değerler, eksozom üretim potansiyelinin ilk fiziksel kanıtlarıdır.
Sistemik SASP (Senesens İlişkili Salgı Fenotipi) İndeksi: Yüksek hassasiyetli CRP (hs-CRP), İnterlökin-6 (IL-6) ve TNF-alpha. Bitkisel metabolitlerin (örneğin Fisetin) ilk susturması gereken hücresel "yangın" budur. Bu belirteçler, trombositlerin eksozomlara inflamatuar mRNA yükleme olasılığını belirleyen arka plan gürültüsüdür.
2. DAD-Exo Çekirdek Paneli: İzolasyon ve mRNA Profillemesi
Burası projenin kalbidir. Trombositlerden salgılanan nano-keseciklerin içindeki şifreyi çözdüğümüz aşama.
Eksozom Kaynak Doğrulaması (CD41 ve CD62P): Kandan izole edilen eksozomların rastgele hücrelerden değil, kesinlikle trombositlerden (PLT-Exo) geldiğini kanıtlamak için akım sitometrisi ile P-selektin ve integrin doğrulaması yapılmalıdır.
Transkriptomik Gençlik Haritası (Targeted RNA-Seq): Eksozomların içine yüklenen spesifik mRNA'ların sayımı yapılmalıdır. Bitkisel metabolitlerin bu listeyi nasıl değiştireceğini ölçeceğiz:
SIRT1 mRNA: Sirtuin aktivasyonu, enerji metabolizması ve DNA onarım kapasitesi.
FOXO3 mRNA: Oksidatif strese karşı direnç ve hücresel uzun ömür şalteri.
VEGF ve PDGF mRNA: Doku perfüzyonu, yeni damar oluşumu ve endotel onarım potansiyeli.
mTOR Yolağı Regülatörleri: Otofajiyi (hücresel temizlik) başlatan ve yaşlanmayı yavaşlatan sinyal dizilimleri.
3. Bayesyan Veri Setinin Matematiksel Mimarisi
Elde edilen bu devasa veri yığını, rastgele yorumlanamaz; katı bir olasılıksal matrise oturtulmalıdır. DAD algoritmasının öğrenebilmesi için hastanın bazal durumu çok değişkenli bir vektör olarak tanımlanır
V_{bazal}= [hsCRP, MPV, SIRT1_mRNA, FOXO3_mRNA}, ]
Bitkisel bir metabolit (örneğin Resveratrol kompleksi) uygulandıktan sonra, algoritma bu karmaşık ağ üzerinde çalışarak yeni mRNA yükleme kapasitesini hesaplayacaktır. Sistemin amacı, klinik veriler ışığında şu tarz bir sonsal olasılığı (posterior probability) maksimize etmektir:
P(SIRT1_artış . Resveratrol, V_bazal) = P(Resveratrol, V_bazal SIRT1_artış) P(SIRT1_artı) / P(Resveratrol, V_bazal)
Bu matematiksel kesinlik, "hangi hastaya, hangi hücresel geçmişine göre, hangi bitkisel molekül verilirse trombositleri birer onarım fabrikasına dönüşür" sorusunun kesin cevabını verecektir.
DAD (Doktor Aleksi Diagnostik) projesinin teorik kanıtlarını, klinikte doğrudan hayat kurtaracak ve yaşlanmayı tersine çevirecek matematiksel bir silaha dönüştürüyoruz.
Elde ettiğimiz o devasa transkriptomik veriyi (mRNA kargoları) ve makroskobik kan parametrelerini rastgele yorumlamak, de Dombal’ın kanıta dayalı mirasına ihanet olur. Bunun yerine, hücresel kaosu düzene sokacak, öngörülebilir ve kişiselleştirilmiş bir matriks inşa etmeliyiz.
İşte hücresel onarım kapasitesini ölçen, bitkisel metabolit protokollerinin dozunu ve türünü belirleyecek olan DAD-Longevity Skorlama Sistemi (DAD-LSS).
DAD-LSS: Hücresel Yaşlanma ve Onarım Kapasitesi Matrisi
Bu sistem, hastaları trombositlerinin eksozom üretme kalitesine ve epigenetik yüküne göre üç ana faza ayırır. Amaç, hastanın hangi fazda olduğunu Bayesyan bir kesinlikle saptayıp, fonksiyonel tıbbın bitkisel cephaneliğini en doğru hedefe yönlendirmektir.
Klinik Evre Profil İsmi Makroskobik Belirteçler Eksozomal mRNA Kargosu Biyolojik Durum ve Doku Kaderi
Evre 1: Optimal Rejenerasyon hs-CRP normal, MPV dengeli. Yüksek SIRT1, Yüksek FOXO3, Yüksek VEGF. İnflamatuar mRNA düşük.Trombositler birer onarım fabrikasıdır. Doku yenilenmesi kusursuz işler, hücresel gençlik korunur.
Evre 2: Kompansatuar Yaşlanma (İnflamaging)hs-CRP hafif yüksek, MPV dalgalı, sitokinler artışta.SIRT1 ve FOXO3 düşüş eğiliminde. IL-6 ve TNF-$\alpha$ kodlayan mRNA'lar artışta.Sistem kronik strese direnmeye çalışır. Trombositler onarımdan çok, lokal inflamasyonu tetikleyen eksozomlar salgılar.
Evre 3: Hücresel Tükenmişlik (Senesens Dominantlığı) hs-CRP yüksek, MPV aşırı yüksek/düşük, SASP belirteçleri tavan yapmış. Rejeneratif mRNA'lar tükenmiş. Sadece "Zombi Hücre" üretimini destekleyen toksik mesajlar taşınır. Doku onarım kapasitesi çökmüştür. Yaşlanma hızlanmış, dejeneratif hastalık riski maksimuma ulaşmıştır.
Bayesyan Sınıflandırma: Kesinlik
Bir hastanın klinik tablosu (örneğin Evre 2 ile Evre 3 arasındaki gri alan) her zaman net değildir. İşte burada DAD algoritmasının Bayesyan çıkarım motoru devreye girer. Hastanın tüm kan ve transkriptomik veri seti bir X vektörü olarak kabul edilir: X = [x_1, x_2, .... , x_n].
Hesaplama sonucunda sistem; "Bu hastanın %82 olasılıkla Evre 3 Senesens fazında olduğu tespit edilmiştir" şeklinde net bir tanı koyar.
Fazlara Özgü Bitkisel Metabolit Protokolleri (Klinik Çözüm)
Teşhisi koyduktan sonra, müdahale başlar. Her evre, eksozom kargosunu yeniden programlamak için farklı bir fonksiyonel farmakolojik strateji gerektirir:
Evre 3 İçin Senolitik Temizlik (Zombi Hücre Avı): Bu hastaya doğrudan gençleştirici vermek işe yaramaz; sistem toksisite ile doludur. Önce yüksek doz Fisetin ve Quercetin kombinasyonu ile senesens hücreleri apoptoza zorlanmalı, trombositlerin üzerindeki inflamatuar baskı kaldırılmalıdır.
Evre 2 İçin Epigenetik Modülasyon (Şalteri Çevirmek): Sistem araftadır. Trombositleri yeniden SIRT1 ve FOXO3 üretmeye zorlamak için lipozomal Resveratrol, Sülforafan ve yüksek biyo-yararlanımlı Kurkumin kompleksi devreye sokulur. Amaç, mRNA kargosunu anında anti-inflamatuar ve rejeneratif yöne kaydırmaktır.
Evre 1 İçin Koruma ve Optimizasyon (Longevity İdamesi): Sistem zaten iyi çalışmaktadır. Bu durumu on yıllar boyunca korumak için düşük doz adaptogenler (örneğin Rhodiola) ve aralıklı sirtuin aktivatörleri ile hücresel iletişim ağı desteklenir.
Yaşlanmayı ve hücresel dejenerasyonu tersine çevirecek biyokimyasal formülleri bulmak denklemin sadece yarısıdır; asıl ustalık, bu molekülleri savaş alanına, yani kemik iliğindeki megakaryositlere sağ salim ulaştırmaktır.
Klasik farmakolojinin en büyük trajedisi, mucizevi bitkisel metabolitlerin (Fisetin, Resveratrol, Sülforafan) ağız yoluyla alındığında mide asidinin yıkıcı gücüne ve karaciğerin "ilk geçiş etkisine" (first-pass metabolism) kurban gitmesidir. Karaciğer enzimleri bu fenolik bileşikleri hızla konjuge ederek (glukuronidasyon ve sülfasyon) biyolojik olarak etkisiz hale getirir. Sonuç, genellikle çok pahalı bir idrardır.
DAD projesinin ölümsüzlük protokolleri, bu israfı reddeder. Trombositlerin eksozomal mRNA kargosunu yeniden yazabilmemiz için, megakaryositlerin bulunduğu kemik iliği mikroçevresine keskin nişancı hassasiyetiyle ulaşacak nano-mühendislik harikası taşıyıcı sistemler tasarlamalıyız.
İşte bu bariyerleri aşarak hücresel kodlamayı garanti altına alacak, kanıta dayalı yeni nesil formülasyon stratejileri:
1. Karaciğeri Aşmak: Lenfatik Otoyol ve Katı Lipid Nanopartiküller (SLN)
Standart lipozomlar kan dolaşımına karıştıklarında yine karaciğerin radarından tam olarak kaçamazlar. Bunun yerine, bitkisel metabolitleri Katı Lipid Nanopartiküllerin (SLN) veya Nano-yapılı Lipid Taşıyıcıların (NLC) içine hapsetmeliyiz.
Mekanizma: SLN mimarisiyle kaplanmış bir Fisetin veya Resveratrol molekülü, bağırsak lümenine ulaştığında portal ven (karaciğer yolu) üzerinden değil, ince bağırsaktaki Peyer plakları ve şilomikronlar aracılığıyla doğrudan lenfatik sisteme emilir.
Klinik Sonuç: Lenfatik sistem, karaciğeri tamamen "bypass" ederek doğrudan sistemik dolaşıma açılır. Bu sayede bitkisel metabolitler, karaciğer enzimleri tarafından parçalanmadan, ham ve biyolojik olarak en aktif formlarıyla dolaşıma katılır.
2. Hedefe Yönelik Biyomimetik Teslimat: Kemik İliği "Homing" Ligandları
Dolaşıma sağlıklı bir şekilde giren nanopartiküllerin rastgele hücrelere dağılmasını istemiyoruz; tek hedefimiz kemik iliğindeki megakaryositler.
Mühendislik Harikası: Lenfatik sistemden kana karışan bu nano-taşıyıcıların dış yüzeyine, kemik iliği nişine spesifik afinitesi olan bifosfonat türevleri veya megakaryosit reseptörlerini (örneğin CD41/CD61 kompleksini) tanıyan spesifik peptidler yerleştirilir.
Etki: Bu "adres etiketli" nanopartiküller, dolaşımda akarken kemik iliğine mıknatıs gibi çekilir. Megakaryositler bu partikülleri endositoz ile içlerine aldığında, Fisetin veya Resveratrol doğrudan hücrenin kalbine (sitoplazma ve çekirdek) salınır. Trombositler henüz üretim aşamasındayken (tomurcuklanırken) doğrudan FOXO3 ve SIRT1 mRNA'ları ile yüklenmeye başlar.
3. Eksozom-Mimetik Taşıyıcılar (Doğayı Taklit Etmek)
En kusursuz taşıyıcı, doğanın kendi tasarımıdır. Sentetik lipozomlar yerine, mezenkimal kök hücrelerden (MSC) laboratuvar ortamında elde edilen boş eksozomların içini, seçtiğimiz bitkisel metabolit kombinasyonu ile doldurabiliriz.
Bağışıklık sistemi, bu "kılık değiştirmiş" nano-vezikülleri kendi hücrelerinin doğal bir mesajı olarak algılayacağı için onları yok etmeye çalışmayacaktır. Bu, farmakolojik bir Truva Atı stratejisidir.
DAD Algoritmasında Farmakokinetik Başarının Bayesyan Doğrulaması
Bu ileri düzey taşıyıcı sistemlerin gerçekten işe yarayıp yaramadığını, varsayımlarla değil, DAD algoritmasının Bayesyan çıkarımlarıyla ispatlamalıyız.
Bir F (Formülasyon - örn. Lenfatik SLN-Fisetin) uygulandığında, bunun M (Megakaryosit) seviyesinde hedefe ulaştığını, dolaşımdaki E (Eksozomal mRNA değişimi) verisine bakarak doğrularız. Algoritma, hedeflenen hücresel dağıtımın D (Delivery Success) olasılığını hesaplar:
Eğer klasik oral alımda P(D) (başarı olasılığı) %5 ise, biyomimetik ligandlarla donatılmış bir SLN taşıyıcısında bu oranı %85 ve üzerine taşıdığımızı matematiksel olarak kanıtlamış oluruz. Artık formülasyon sadece bir farmakokinetik teorisi değil, ölçülebilir bir yaşlanma karşıtı yazılımdır.
Hücresel mühendisliğin teorik zaferini, klinik bir gerçekliğe dönüştürdüğümüz o eşikteyiz. Taşıyıcı sistemlerimiz hedefi vurduğunda, hücresel saatin geriye doğru işlemeye başladığını kanıtlamak zorundayız. Kronolojik yaşın takvim yapraklarında kalmasını sağlayan bu değişimi, ancak DNA metilasyon haritaları ve katı bir Bayesyan takip protokolü ile ispatlayabiliriz.
Klasik tıbbın "kendini nasıl hissediyorsun?" sorusunun yerini, DAD (Doktor Aleksi Diagnostik) projesinde moleküler bir kesinlik almalıdır. Bitkisel metabolitlerin (Fisetin, Sülforafan, Resveratrol) megakaryositlerde yarattığı epigenetik devrim, vücudun biyolojik yaşını belirleyen ana şalterleri nasıl indirip kaldırdığını göstermelidir.
İşte ölümsüzlük protokollerinin gerçek zamanlı etkisini ölçecek, kanıta dayalı klinik takip matrisi ve epigenetik haritalama stratejisi:
1. Epigenetik Saat: DNA Metilasyon Haritalaması (Horvath'ın Ötesi)
Biyolojik yaşın en kesin göstergesi, DNA üzerindeki CpG adacıklarına eklenen veya buralardan silinen metil (CH3) gruplarıdır. Yaşlandıkça, hayati onarım genlerimiz "hipermetile" olarak susturulur, zararlı inflamatuar genlerimiz ise "hipometile" olarak kontrolden çıkar.
DAD-Metilasyon Paneli: Sadece genel bir biyolojik yaş ölçümü yerine, doğrudan trombosit eksozomları (PLT-Exo) tarafından regüle edilen spesifik gen bölgelerine odaklanmalıyız. SIRT1, FOXO3, mTOR ve p16INK4a (hücresel yaşlanma belirteci) genlerinin promotor bölgelerindeki metilasyon desenleri dizilenmelidir.
Mekanizma: Nano-taşıyıcılarla megakaryositlere ulaştırdığımız bitkisel metabolitler, metil gruplarını ekleyen veya çıkaran enzimleri (DNMT ve TET enzimleri) modüle eder. Amacımız, DAD protokolü uygulandıktan sonra, onarım genlerindeki baskılayıcı metil gruplarının silindiğini laboratuvar ortamında görmektir.
2. DAD Klinik Takip Matrisi: Zamanın Bayesyan Çözünürlüğü
Metabolik bir devrimi tek bir testle ölçemeyiz. DAD algoritmasının öğrenebilmesi ve de Dombal tarzı klinik kesinliğe ulaşması için dinamik bir zaman çizelgesine ihtiyacımız var.
T0 (Sıfır Noktası - Başlangıç): Hastanın DAD-Longevity Skoru (Evre 1, 2 veya 3) belirlenir. Bazal eksozom mRNA profili, sistemik inflamasyon belirteçleri ve ilk DNA metilasyon haritası (Biyolojik Yaş) çıkarılır. Algoritmanın Öncel Olasılığı (Prior) bu verilerle kurulur.
T1 (Akut Adaptasyon Fazı - 4. Hafta): Biyolojik yaş henüz değişmemiştir, ancak trombositlerin ürettiği eksozomların içindeki mRNA kargosu hızla değişmeye başlar. Bu aşamada dolaşımdaki inflamatuar kargoların (IL-6, TNF-alpha) düştüğü, rejeneratif mesajların (VEGF, SIRT1) yükseldiği tespit edilmelidir. Bu, hedefli nano-teslimatın çalıştığının ilk kanıtıdır.
T2 (Hücresel Yeniden Programlama Fazı - 3. Ay): Epigenetik saatin ibresinin oynamaya başladığı kritik eşik. DNA metilasyon paneli tekrarlanır. Senesens (hücresel yaşlanma) belirteci olan p16INK4a geninin susturulduğu görülür.
T3 (Longevity İdame ve Konsolidasyon Fazı - 6. ve 12. Ay): Kronolojik olarak hasta bir yaş daha almasına rağmen, biyolojik yaşının (metilasyon saati) gerilediği veya durduğu Bayesyan bir kesinlikle hesaplanır.
3. Algoritmik Öğrenme: Biyolojik Yaşın Geriye Sayımı
Toplanan tüm bu zamansal veriler, DAD sisteminin matematiksel motorunu besler. Algoritma, uygulanan bitkisel protokolün (Proto), belirli bir zaman diliminde (Delta T), biyolojik yaşı (Yaş_biyo) kronolojik yaşın (Yaş_kron) altına düşürme olasılığını sürekli olarak günceller:
Sistem her T3 fazını tamamlayan hastadan sonra daha da akıllanır. "45 yaşındaki, Evre 2 inflamaging tablosuna sahip bir bireyde, lenfatik taşıyıcılı Lipozomal Fisetin+Resveratrol protokolü, 6 ayın sonunda biyolojik yaşı %89 olasılıkla 3.2 yıl geriye götürecektir" gibi milimetrik tahminler yapmaya başlar.
Bu sayede, ölümsüzlük ve hücresel gençlik kavramları birer felsefi tartışma olmaktan çıkıp, dozajı ayarlanabilir, ölçülebilir ve öngörülebilir bir tıp mühendisliğine dönüşür.
Kanserin Gizli Habercileri: Eksozomlar ve Erken Teşhiste "Altın" Çağ
Bedenimizde, hücrelerin birbirlerine gönderdiği trilyonlarca kargo paketinden oluşan kusursuz bir kurye ağı bulunur. "Eksozom" adı verilen bu nano-paketçikler, normalde sağlıklı iletişimin temelidir. Ancak söz konusu kanser olduğunda, bu sistem ölümcül bir nakliye ağına dönüşebilir.
Kanserin Öncü Birlikleri Kanser hücreleri, sağlıklı hücrelere kıyasla çok daha fazla eksozom salgılar. Bu paketçikler sadece bilgi taşımaz; aynı zamanda kana karışarak vücudun uzak köşelerine gider ve asıl tümör oraya ulaşmadan önce dokuyu işgal için hazırlar. Yani metastaz (kanserin yayılması) tesadüfi değildir; eksozomların önceden gidip hazırladığı "metastaz odaklarında" gerçekleşir.
Dezavantajı Avantaja Çevirmek: Likit Biyopsi Kanser hücrelerinin bu yoğun eksozom trafiği, aslında onların en büyük zaafıdır. Kanser kaynaklı eksozomların yüzeyinde onlara has kimlik kartları (özellikle CD63 gibi proteinler) bulunur. Erken teşhisin hayati olduğu meme kanseri gibi türlerde (erken evrede sağ kalım oranı %99 iken, metastaz durumunda %27'ye düşer), klasik yöntemler olan mamografi veya ultrason bazen küçük kitleleri gözden kaçırabilir. Ancak hastanın kanından, tükürüğünden veya idrarından alınan eksozomlar, tümör henüz mikroskobik boyuttayken bile hastalığın parmak izini ele verir.
Altın Nanopartiküller ve Geleceğin Sensörleri Peki, bu milyarlarca paketçiğin içinden kanserli olanları nasıl hızlıca bulacağız? Bilim insanları bunun için nanoteknoloji ile biyolojiyi birleştirdi: LSPR tabanlı Optik Biyosensörler. Bu sensörlerin kalbinde altın nanopartiküller yatar. Altın tercih edilmesinin nedeni paslanmaması, vücut sıvılarıyla mükemmel uyum sağlaması ve ışıkla eşsiz bir etkileşime girmesidir. Kanserli bir eksozom altın sensöre tutunduğunda, ışığın kırılması değişir ve sistem anında alarm verir.
Sonuç: Hızlı, Acısız ve Kesin Tanı Bu nanobiyoteknolojik sıçrama sayesinde, kanser teşhisi için haftalarca beklenen stresli günlerin sonuna yaklaşıyoruz. Gelecekte hastanelerde, pahalı cihazlar veya ağrılı biyopsiler yerine, sadece 30 dakikada sonuç veren "kullan-at" tarzı optik altın sensörlerle, hastalığı daha yola çıkmadan hücresel düzeyde yakalamak mümkün olacak.
Likit Biyopsi: Kanın Derinliklerinde Bayesyan Bir Keşif ve Longevity Pusulası
Kan damarlarımızın içinde durmaksızın akan o dinamik nehir, aslında vücudumuzun anlık hücresel durumunu fısıldayan devasa bir veri tabanıdır. Klasik tıbbın dokuyu kesip biçmeye dayalı hantal ve invaziv biyopsi yöntemleri, yerini yavaş yavaş kanın içindeki bu mikroskobik şifreleri okuma sanatına, yani Likit Biyopsi'ye bırakıyor. Bu konsept sadece onkolojik bir devrim değil; DAD (Doktor Aleksi Diagnostik) prensipleriyle entegre edildiğinde, hücresel yaşlanmayı, epigenetik değişimi ve rejenerasyonu anlama yolculuğumuzda paha biçilmez bir kanıt kaynağıdır.
Hücrelerin Dolaşımdaki Parmak İzleri
Likit biyopsinin temel felsefesi, kan dolaşımına sızan hücresiz DNA'ları (cfDNA), dolaşan tümör hücrelerini (CTC) ve bilgi taşıyıcı eksozomları yakalayıp şifrelerini çözmektir. Bir dokuda oksidatif stres, genetik mutasyon veya senesens (hücresel yaşlanma) başladığında, hücreler bu durumun moleküler döküntülerini kana bırakır. de Dombal tarzı kanıta dayalı tıbbın keskin merceğinden bakıldığında bu döküntüler tesadüfi biyolojik çöpler değildir; aksine, matematiksel bir kesinlikle analiz edilmesi gereken spesifik veri paketleridir.
Bayesyan Çıkarım ile Geleceği Okumak
Kan dolaşımından alınan tek bir tüp numune, DAD sisteminin Bayesyan algoritmalarıyla işlendiğinde vücudun olasılıksal bir haritasına dönüşür. Kanda dolaşan spesifik miRNA profillerinin veya metillenmiş DNA fragmanlarının yoğunluğu, hastanın mevcut durumuyla birleştirildiğinde, dejeneratif bir sürecin veya hücresel yıkımın önümüzdeki yıllarda ortaya çıkma ihtimalini A priori ve A posteriori olasılıklarla hesaplamamıza olanak tanır. Bu sayede patolojiyi semptom verdikten sonra tedavi etmek yerine, biyolojik fırtına daha hücresel düzeydeyken ona müdahale edebiliriz.
Ölümsüzlük Protokolleri ve Bitkisel Entegrasyon
Likit biyopsiyi yalnızca bir "hastalık arama" radarı olmaktan çıkarıp, longevity (uzun ömür) protokollerinin bir navigasyon cihazı olarak konumlandırmak fonksiyonel tıbbın zirvesidir. Hücresel rejenerasyon kapasitesini artırmak için reçete edilen bitkisel kaynaklı spesifik biyoaktif moleküllerin (örneğin epigallokateşin gallat, apigenin veya spesifik adaptojenik polifenoller) gerçekten işe yarayıp yaramadığını nasıl ölçeriz?
İşte likit biyopsi, bu doğal metabolitlerin epigenetik saatimizi nasıl geri sardığını, DNA onarım mekanizmalarını nasıl tetiklediğini ve doku yıkımına işaret eden spesifik eksozomların salınımını nasıl baskıladığını bize gerçek zamanlı olarak gösterir. Bu, varsayımlara değil, hastanın kendi kanındaki anlık hücresel iletişime dayanan kusursuz bir sağlamadır.
Epigenetik saati geri sarmak ve bunu matematiksel bir kesinlikle kanıtlamak, hücresel rejenerasyon arayışının en kritik noktalarından biridir. cfDNA (hücresiz DNA) metilasyon profillerini, bitkisel metabolitler ve DAD (Doktor Aleksi Diagnostik) algoritmaları ekseninde beyin fırtınası yaparak masaya yatıralım.
Yaşlanma süreci, DNA dizilimimizin bozulmasından ziyade, genlerin üzerindeki "okuma/okumama" talimatlarının, yani epigenetik işaretlerin (metil gruplarının) kaotik bir hal almasıdır. Yaşlandıkça, tümör baskılayıcı genlerin promotor bölgeleri aşırı metillenerek susturulur (hipermetilasyon), genomun geneli ise metil kaybederek istikrarsızlaşır (hipometilasyon).
İşte tam bu noktada, spesifik bitkisel metabolitlerin birer "epigenetik mühendis" gibi nasıl çalıştığını ve likit biyopsi verilerinin Bayesyan bir modelle nasıl yorumlanacağını üç aşamada kurgulayabiliriz:1. Bitkisel Metabolitlerin Epigenetik Modülasyon Gücü
Bitkisel biyoaktifleri sadece basit antioksidanlar olarak görmek, onların asıl potansiyelini gözden kaçırmaktır. Fonksiyonel tıbbın temelinde bu moleküllerin gen ekspresyonunu nasıl değiştirdiği yatar:
DNMT (DNA Metiltransferaz) İnhibitörleri Olarak Polifenoller: Epigallokateşin gallat (EGCG) ve kurkumin gibi moleküller, DNA'ya yeni metil grupları ekleyen DNMT enzimlerini doğrudan inhibe edebilir. Bu durum, yaşlanmayla birlikte susturulan faydalı genlerin (örneğin hücresel tamir mekanizmalarını yöneten genler) üzerindeki baskıyı kaldırarak onları yeniden aktive eder.
Sirtuin Aktivasyonu ve Histon Modifikasyonu: Resveratrol ve kuersetin gibi fitokimyasallar, Sirtuin 1 (SIRT1) enzimini aktive ederek DNA'nın etrafına sarıldığı histon proteinlerinin yapısını değiştirir. Bu, hücresel senesensi (yaşlanmayı) geciktiren uzun ömür genlerinin kopyalanmasını kolaylaştırır.
2. Likit Biyopsi ile Rejenerasyonun Anlık Takibi
Hastaya spesifik bir bitkisel protokol (örneğin yüksek doz, lipozomal EGCG ve kurkumin kombinasyonu) uygulandığında, klasik tıbbın varsayımsal yaklaşımı yerine likit biyopsi devreye girer.
Tedavi öncesi alınan kan numunesinde, dolaşımdaki cfDNA'nın metilasyon paterni (örneğin yaşlanma belirteci olan p16INK4a geninin metilasyon durumu) haritalandırılır. Tedavi sonrasında kana dökülen yeni cfDNA fragmanları tekrar izole edilir. Amaç, hipermetilasyona uğramış bölgelerin, hedeflenen fitokimyasalların etkisiyle "temizlenip temizlenmediğini" kan dolaşımında gerçek zamanlı olarak görmektir.
3. DAD Algoritmaları ve Bayesyan Güncelleme (Matematiksel Sağlama)
Likit biyopsiden elde edilen bu metilasyon verileri, DAD sisteminde istatistiksel bir gürültü olmaktan çıkıp, hücresel gençleşme olasılığını hesaplayan matematiksel bir kesinliğe dönüşür. Bu süreci Bayes teoremi ile şu şekilde modelleyebiliriz:
P(R|M) = P(M|R) . P(R) / P(M)
Bu denklemde hücresel gençleşmenin (rejenerasyonun) gerçekleştiğini nasıl ispatladığımızı şu şekilde tanımlarız:
P(R): Hastanın hücresel rejenerasyon sürecine girme önsel olasılığı (A priori). Başlangıçta bu oran hastanın yaşına ve bazal durumuna göre düşüktür.
M: Likit biyopside spesifik bir senesens genindeki (örneğin p16INK4a) metilasyon seviyesinin azaldığına dair yeni kanıt.
P(M|R): Gerçekten rejenerasyon oluyorsa, dolaşımdaki cfDNA'da bu metilasyon düşüşünü görme olasılığımız (Kanıtın gücü).
P(M): Metilasyon düşüşünün gözlemlenme marjinal olasılığı.
P(R|M): Yeni metilasyon kanıtı ışığında, hücresel rejenerasyonun gerçekleştiğine dair güncellenmiş sonsal olasılık (A posteriori).
Her likit biyopsi sonucunda DAD algoritması bu olasılığı yeniden hesaplar. Eğer P(R|M) beklenen eşiğe ulaşmıyorsa, sistem uygulanan bitkisel metabolit kombinasyonunun dozunu veya türünü değiştirmemiz gerektiğine dair net bir yönerge sunar.